题目内容
【题目】过氧化钙(CaO2)广泛应用于水产养殖、污水处理等领域,是优良的供氧剂。
【资料】过氧化钙(CaO2)常温下能与水反应生成氢氧化钙和氧气。
【探究一】证明某种供氧剂的主要成分为过氧化钙
(1)取一定量该供氧剂放置于试管中,向其中加水,再将带火星的木条伸入试管口中,观察到____,证明该供氧剂的主要成分为过氧化钙。
(2)此供氧剂的保存方法是______。
(3)此供氧剂长期暴露在空气中,会变质生成CaCO3。为检验此供氧剂是否变质,可向其加入稀盐酸,若观察到有气泡生成,则判断此供氧剂已变质。你是否认同上述方案,理由___。
【探究二】此类供氧剂中过氧化钙(CaO2)的含量测定
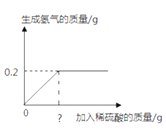
【方案一】通过测定产生氧气的体积,最终计算出供氧剂中过氧化钙的含量。
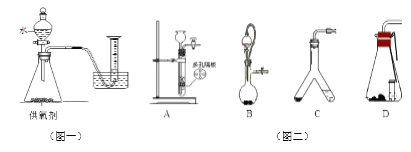
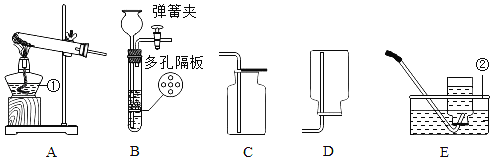
(1)取一定质量的供氧剂溶于水,按照图一装置进行装配。充分反应后,待量筒中液面不再变化,还要______,再读出体积。
(2)为保证测量结果的准确性,收集气体的时机是___________。
a.导管口还没有气泡产生时 b.导管口连续均匀冒出气泡时
c.导管口冒出气泡很多时
(3)用此装置测得的含量会偏大,如果将发生装置换成图二中的装置__________(填序号)可以避免此误差。
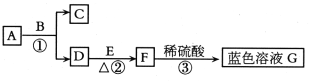
【方案二】把样品中的过氧化钙转化为碳酸钙,通过测定碳酸钙沉淀的质量,进而求得过氧化钙的质量。具体流程如下图:

(1)写出供氧剂与水反应的化学方程式__________;
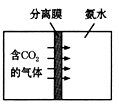
(2)滴加的Na2CO3溶液要过量的原因是 __________;
(3)洗涤沉淀的目的是 __________;
(4)检验沉淀已经洗涤干净的方法是:取最后一次洗涤液,滴加_____溶液,若无明显现象,则表示已经洗净。
(5)若供氧剂的质量m=5 g, 碳酸钙质量n=5 g,请通过计算得出供氧剂中的过氧化钙的含量。__________________(实验过程)
(6)若CaCO3沉淀过滤后不洗涤,则过氧化钙的含量将 ______ (填“偏大”、“偏小”或“无影响”)。
(7)此方案排除所加试剂和操作的原因,测定的过氧化钙含量也可能偏大,原因是___ 。
【答案】 带火星的木条复燃 密封、干燥保存 不认同,因为盐酸中的水与CaO2反应会生成O2,即使没有CaCO3与盐酸反应生成CO2,也会有气泡生成。 使量筒内外液面相平 a BCD 2CaO2+2H2O=2Ca(OH)2+O2↑ 使氯化钙完全转化为沉淀 除去沉淀表面的可溶性杂质,测量结果更准确 硝酸银溶液 72.0% 偏大 所测样品中Ca元素还可能还来源于变质生成的Ca(OH)2、CaCO3,从而所测过氧化钙含量偏大。
【解析】探究一(1)根据氧气能使带火星的木条复燃解答;(2)根据物质的性质可以判断保存方法;(3)根据水与CaO2反应会生成O2分析解答;探究二【方案一】(1)根据量筒内外液面相平解答;(2)为保证测量结果的准确性,收集气体的时机是导管口还没有气泡产生时,因为这样不会导致生成的气体损失,全面进入量筒中;(3)根据导致测得的含量偏大的原因是分液漏斗中滴下的水会占据一部分体积,导致测定的氧气体积偏大解答;【方案二】(1)根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式;(2)滴加的Na2CO3溶液要过量的原因是使氯化钙完全反应;(3)根据除去沉淀表面的可溶性杂质,测量结果更准确解答;(4)根据氯化钠能和硝酸银反应生成白色沉淀氯化银和硝酸钠解答;(5)根据提供的数据和反应的化学方程式可以进行相关方面的计算;(6)根据CaCO3沉淀过滤后不洗涤,会导致碳酸钙质量偏大,从而导致过氧化钙含量偏大;(7)根据过氧化钙可能变质解答。探究一(1)取一定量该供氧剂放置于试管中,向其中加水,再将带火星的木条伸入试管口中,观察到带火星的木条复燃,证明该供氧剂的主要成分为过氧化钙;(2)此供氧剂能和水反应,因此保存方法是密封、干燥保存;(3)不认同;因为盐酸中的水与CaO2反应会生成O2,即使没有CaCO3与盐酸反应生成CO2,也会有气泡生成,因此不能通过观察到有气泡生成来判断此供氧剂已变质;探究二【方案一】(1)取一定质量的供氧剂溶于水,按照图一装置进行装配。充分反应后,待量筒中液面不再变化,还要使量筒内外液面相平,再读出体积;(2)为保证测量结果的准确性,收集气体的时机是导管口还没有气泡产生时。故选a;(3)用此装置测得的含量会偏大,是因为分液漏斗中滴下的水会占据一部分体积,导致测定的氧气体积偏大,从而导致测定的结构偏大;如果将发生装置换成图二中的装置BCD装置可以避免此误差;【方案二】(1)供氧剂与水反应的化学方程式为2CaO2+2H2O=2Ca(OH)2+O2↑;(2)滴加的Na2CO3溶液要过量的原因是使氯化钙完全转化为沉淀;(3)洗涤沉淀的目的是除去沉淀表面的可溶性杂质,测量结果更准确;(4)检验沉淀已经洗涤干净的方法是:取最后一次洗涤液,滴加硝酸银溶液,若无明显现象,则表示已经洗净;(5)设过氧化钙质量为x。
由2CaO2+2H2O=2Ca(OH)2+O2↑,CO2+Ca(OH)2=CaCO3↓+H2O可知,CaO2~CaCO3。
CaO2~CaCO3
72 100
x 5g![]()
x=3.6g
供氧剂中的过氧化钙的含量为![]() ×100%=72.0%;
×100%=72.0%;
(6)若CaCO3沉淀过滤后不洗涤,则会导致碳酸钙质量偏大,从而导致计算的过氧化钙质量偏大,进一步导致过氧化钙的含量将偏大;(7)此方案排除所加试剂和操作的原因,测定的过氧化钙含量也可能偏大,原因是所测样品中Ca元素还可能还来源于变质生成的Ca(OH)2、CaCO3,从而导致所测过氧化钙含量偏大。

【题目】(10分)兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验:
(1)氢氧化钠固体要密封保存,原因有:
① ;② 。
【对固体猜想】
猜想一:全部是NaOH;猜想二:全部是Na2CO3;猜想三:是NaOH和Na2CO3混合物
【实验和推断】(2)为进一步确定成分,进行了以下探究:
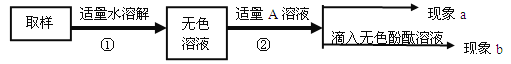
对无色溶液进行以下实验:
实验操作 | 实验现象 | 实验结论 |
第一步: 用试管取约2mL该溶液,滴入适量氢氧化钙溶液,振荡。 | 现象a:白色沉淀 | 化学方程式: ① , 有碳酸钠并全部除尽。 |
第二步: 静置,取上层清液于试管中滴入酚酞溶液,振荡。 | 现象b: ② | 含有NaOH,猜想三成立,是NaOH和Na2CO3混合物 |
③分析:小组中有同学提出质疑,认为以上实验不能证明猜想三成立,理由是:
。
④反思:把第一步中的氢氧化钙溶液换成 溶液,可达到实验目的。
(3)请利用以下提供的试剂,设计实验证明猜想一是正确的,即氢氧化钠没有变质。
提供的试剂有:酚酞溶液、稀盐酸、氢氧化钡溶液、氯化钡溶液
实验操作 | 实验现象 | 实验结论 |