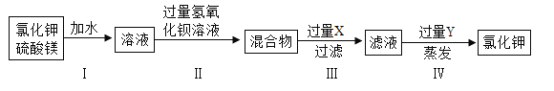
题目内容
【题目】3 月 22 日是“世界水日”,水与人类的生活和生产密切相关
(1)生活中存在硬水和软水,可以用_____区分硬水和软水。
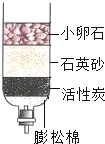
(2)硬水给生活和生产带来很大的不利,生活中通过_____可以降低水的硬度。如图是小芳同学自制简易净水装置,其中石英砂的作用是_____。
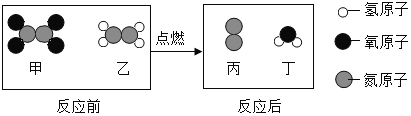
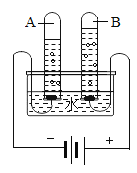
(3)在研究水的组成时,先将水电解(装置如右图所示),A 中的气体是____________(填名称),充分反应后 A 中气体与 B 中气体的体积比是______________,反应原理____________________(请用化学方程式书写),该实验说明水是______由组成的。
(4)日常生活中你经常采用的节约用水的措施是_______________。
【答案】肥皂水 煮沸 过滤 氢气 2 :1 2H2O ![]() 2H2↑﹢O2↑ 氢元素和氧元素 淘米水浇花
2H2↑﹢O2↑ 氢元素和氧元素 淘米水浇花
【解析】
(1)生活中存在硬水和软水,可以用肥皂水区分硬水和软水。将其分别混合后,搅拌,浮渣多,泡沫少的是硬水,反之是软水;
(2)硬水给生活和生产带来很大的不利,生活中通过加热、煮沸可以降低水的硬度。因为在煮沸过程中,钙、镁离子会形成沉淀,自制简易净水装置,其中石英砂阻挡大颗粒物质通过,但液体可以通过,作用是:过滤。
(3)在研究水的组成时,先将水电解正极产生氧气,负极产生氢气,A 试管连接电源负极,产生的气体是氢气,充分反应后 氢气与氧气的气体的体积比是2:1,水通电产生氢气和氧气的化学方程式:2H2O ![]() 2H2↑﹢O2↑,该实验说明水是由氢元素和氧元素组成的。
2H2↑﹢O2↑,该实验说明水是由氢元素和氧元素组成的。
(4)日常生活中经常采用的节约用水的措施是:淘米水浇花等。

【题目】在一次实验课上,同学们用碳酸钠溶液鉴别氯化钙溶液和稀盐酸,实验结束后将试管中的物质倒入同一洁净的烧杯中,得到无色溶液(如图所示)。
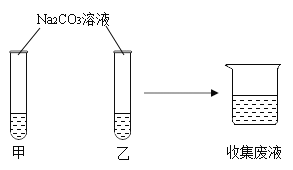
(1)如果试管甲中观察到有白色沉淀生成,则试管乙中发生反应的化学方程式为_______________。
(2)为处理实验废液,小组同学对废液成分进行探究:
[提出问题]假设二氧化碳全部逸出,废液中的溶质是什么?
[分析]小涛认为一定有氯化钠,其依据是_________________。
[猜想]可能有HCI、Na2CO3、CaCl2中的一种或两种。
[设计实验](本环节可供选择的试剂有稀HCI、Na2CO3溶液、CnCl2溶液、铁粉)
步骤 | 操作 | 现象 | 结论 |
① | 取烧杯中溶液样品,加入铁粉 | _________ | 溶液中含有HCl |
② | 取烧杯中溶液样品,滴加氯化钙溶液 | 无明显现象 | 溶液中不含Na2CO3 |
③ | __________________________ | _________________ | 溶液中含有CaCl2 |
[结论]废液中的溶质是HCI、NaCl、CaCl2。
[反思]小梅认为根据步骤①的现象,步骤②可以省略,原因是___________。
[应用]本实验废水直接排放,造成的影响是____________(写一种即可),若在不使用其他药品时,将实验后废液处理成中性后排放,在氢氧化钠、生石灰、石灰石三种物质中,应该选择______________。