题目内容
【题目】工业生产的氯化钾中含有少量硫酸镁杂质,实验窒为提纯氯化钾,设计的实验念过程如下图所示:
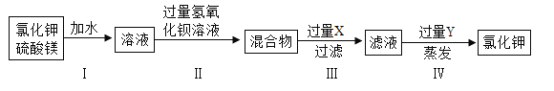
(1)写出步骤Ⅱ中发生反应的化学方程式________________________。
(2)提纯过程所用试剂ⅹ、Y分别是(写溶质化学式)_______________、______________。
【答案】MgSO4+Ba(OH)2=Mg(OH)2↓+BaSO4↓ K2CO3 HCl
【解析】
(1)根据流程图可知,步骤Ⅱ中反应的化学反应是硫酸镁和氢氧化钡反应生成硫酸钡沉淀和氢氧化镁沉淀,化学方程式为:MgSO4+Ba(OH)2=Mg(OH)2↓+BaSO4↓。故填:MgSO4+Ba(OH)2=Mg(OH)2↓+BaSO4↓。
(2)加入过量的X是为了除去多余的氢氧化钡溶液,因此加入的试剂X时K2CO3,碳酸钾可和氢氧化钡反应生成碳酸钡沉淀和氢氧化钾,加入过量的Y是为了除去过量的K2CO3以及生成的KOH,因此Y是稀盐酸,稀盐酸和碳酸钾反应生成氯化钾和二氧化碳以及水,氢氧化钾和稀盐酸反应生成氯化钾和水,过量的稀盐酸在蒸发过程中挥发出去,最终得到氯化钾晶体。故填:K2CO3;HCl。

练习册系列答案
相关题目