题目内容
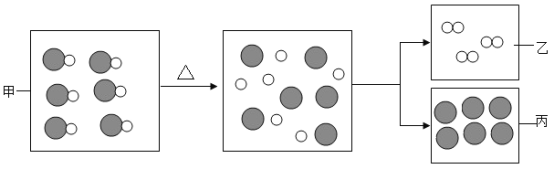
【题目】新型药膏辅料生产中常常需要氧化锌作添加剂。由工业锌粉生产活性ZnO的部分生产流程如下:
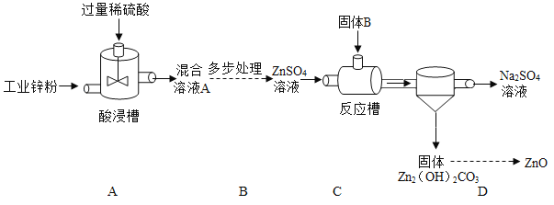
(1)A中发生反应的化学方程式为______。B过程处理主要目的是______。
(2)混合溶液A中一定含有的阳离子是_____。
(3) D中的实验操作是_____。
(4)加入的固体B是______。
【答案】Zn+H2SO4═ZnSO4+H2↑ 除去过量的硫酸 ![]() 过滤 Na2CO3
过滤 Na2CO3
【解析】
根据A中锌与稀硫酸反应,稀硫酸过量所以A中的溶质有两种;B处后只有溶质硫酸锌,所以B主要是除去硫酸;观察图中固体与溶液分离,应是过滤;再利用质量守恒定律进行分析作答。
(1)A中锌能与过量稀硫酸反应生成硫酸锌和氢气,反应的化学方程式为Zn+H2SO4═ZnSO4+H2↑;由于加入了过量稀硫酸,B过程处理主要目的是除去过量的硫酸。
(2)由于稀硫酸过量,所以A是硫酸和硫酸锌的混合溶液,一定含有的阳离子是氢离子和锌离子;
(3)D是将固体与溶液分离,所以操作是过滤;
(4)由于D中得到的是固体碱式碳酸锌和硫酸钠,生成物中有碳元素和钠元素,根据质量守恒定律,B的成分可能是Na2CO3,因为碳酸钠溶液显碱性,可能和硫酸锌反应生成碱式碳酸锌和硫酸钠。

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
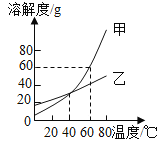
【题目】NH4Cl和Na2SO4的溶解度表及溶解度曲线如下。下列说法正确的是 ( )
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度S/g | NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 60.2 |
Na2SO4 | 9.6 | 20.2 | 40.8 | 48.4 | 47.5 | 47.0 | |
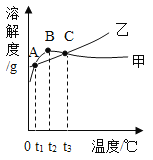
A.甲为NH4Cl
B.t2℃应介于30℃~50℃
C.甲、乙饱和溶液从t3℃降温到t2℃,溶质的质量分数都变小
D.等质量的甲、乙饱和溶液从t1℃升温到t3℃,为使其溶液恰好饱和,加入的甲、乙固体质量相等