题目内容
【题目】某同学将如下实验一反应后的物质和实验二反应后的硬质玻璃管中的物质倒入同一个容器内,发现有化学反应发生,于是便对容器内反应后的物质成分探究产生了兴趣。
(查阅资料):Fe2O3 + 6HCl = 2FeCl3 + 3H2O
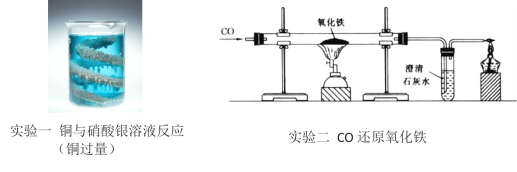
(讨论分析)同学们经过讨论分析,认定该容器内物质混合后会发生化学反应,化学方程式为______.
(设计实验)为进一步确定容器内物质成分,同学们做了以下探究,请完成填空。
实验步骤 | 实验现象 | 实验结论 |
一、把容器内的混合物过滤,得到固体和溶液,将固体烘干,用磁铁吸引固体。 | ___________ | 固体中不含铁。 |
二、取少量步骤一固体,加入过________。 | 固体粉末减少,溶液变成黄色 | 固体中一定含有_________。 |
三、___________ | ___________ | 溶液中含有硝酸铜 |
(问题探讨)混合物中不含单质铁的原因是___________。
【答案】Fe+Cu(NO3)2 =Fe(NO3)2+Cu 磁铁上没有固体被吸引 稀盐酸 氧化铁 取少量步骤一的滤液,加入洁净的铁片 铁片表面生成红色固体,溶液由蓝变绿 实验一中生成的硝酸铜与实验二生成的铁发生了置换反应
【解析】
{讨论分析}反应是铁与硝酸铜反应生成硝酸亚铁和铜,故反应的化学方程式写为:Fe+Cu(NO3)2 =Fe(NO3)2+Cu。
{实验设计}固体中不含铁,用磁铁吸引,会看到磁铁上没有固体被吸引,故填磁铁上没有固体被吸引;
氧化铁与盐酸反应生成氯化铁,氯化铁溶于水后溶液呈黄色,故填稀盐酸;
固体与盐酸反应生成氯化铁,氯化铁溶于水后溶液呈黄色,则固体中一定有氧化铁,故填氧化铁;
检验溶液中含有硝酸铜的方法是取少量步骤一的滤液,加洁净的铁片,故填取少量步骤一的滤液,加洁净的铁片;
铁与硝酸铜溶液反应的现象可以看到:铁片表面生成红色固体,溶液由蓝变绿,故填铁片表面生成红色固体,溶液由蓝变绿。
{问题讨论}混合物中不含单质铁的原因是实验一中生成的硝酸铜与实验二生成的铁发生了置换反应,故填实验一中生成的硝酸铜与实验二生成的铁发生了置换反应。

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案