题目内容
学习酸碱中和反应时,很多同学对其产生探究兴趣。
(1)甲同学将固体氢氧化钠放入装有稀硫酸的试管中并振荡,试管壁发烫,于是他得出酸碱中和反应是放热反应的结论。乙同学认为甲同学的推理不合理,理由是________________ __。
(2)乙同学为了验证甲同学的结论,将实验加以改进:将稀硫酸慢慢滴入装有氢氧化钠溶液的烧杯中,氢氧化钠溶液的温度随着加入的稀硫酸质量的变化曲线如下图所示:
①由该图知,稀硫酸与氢氧化钠溶液发生的
反应是____ ___ (填“放热”或“吸
热”)反应,B点表示的含义是______________。
②A→B,烧杯中溶液的pH逐渐____________。
③B→C,烧杯内溶液中含有的阳离子有________(填离子符号)。
(3)丙同学将稀硫酸滴入氢氧化钠溶液中,有气
泡产生,他认为氢氧化钠溶液已变质。请你分析
变质的原因(用化学方程式表示)_____________ ____。
(4)丁同学认为氢氧化钠溶液与稀硫酸混合没有明显现象,于是他想借助下列溶液来验证反应是否真的发生,你觉得不可行的是________________________。
A.无色酚酞试液 B.FeCl3 C.BaCl2 D.KNO3

(1)固体氢氧化钠溶于水放热 (2)①放热 酸碱恰好完全中和 ②减小
③Na+、H+ (3)2NaOH+CO2 Na2CO3+H2O (4)CD
Na2CO3+H2O (4)CD
解析:(1)甲同学的操作包括了氢氧化钠固体的溶解过程以及氢氧化钠与稀硫酸反应的过程,故不能得出中和反应是放热反应的结论。(2)①根据图像可以看出随着稀硫酸的加入温度在逐渐上升,B点是温度的转折点,也是反应的转折点。②A→B:稀硫酸与氢氧化钠反应,溶液由碱性逐渐变为中性,pH逐渐减小。③B→C:稀硫酸与氢氧化钠完全反应后,继续加入稀硫酸,稀硫酸过量。(3)氢氧化钠与空气中的二氧化碳反应生成碳酸钠和水。(4)无论二者是否反应,钡离子与硫酸根离子会发生反应生成硫酸钡沉淀;钾盐和硝酸盐都溶于水,在水中起不到指示剂的作用。

 阅读快车系列答案
阅读快车系列答案 (2010?宿迁)学习酸碱中和反应时,很多同学对其产生探究兴趣.
(2010?宿迁)学习酸碱中和反应时,很多同学对其产生探究兴趣. 33、学习酸碱中和反应时,很多同学对其产生探究兴趣.
33、学习酸碱中和反应时,很多同学对其产生探究兴趣.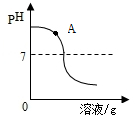 (2012?浦东新区二模)在学习酸碱中和反应时,同学们做了稀硫酸和氢氧化钠溶液反应的实验.
(2012?浦东新区二模)在学习酸碱中和反应时,同学们做了稀硫酸和氢氧化钠溶液反应的实验. 在学习酸碱中和反应时,同学们做了稀硫酸和氢氧化钠溶液反应的实验.
在学习酸碱中和反应时,同学们做了稀硫酸和氢氧化钠溶液反应的实验.