题目内容
【题目】元素周期表第三周期的七种元素的有关数据如表:
元素名称 | 钠 | 镁 | 铝 | 硅 | 磷 | 硫 | 氯 |
核电荷数 | 11 | 12 | 13 | 14 | 15 | 16 | 17 |
常见化合价 | +1 | +2 | +3 | -4、+4 | -3、+5 | -2、+4、+6 | -1、+7 |
最外层的电子数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
(1)用化学符号表示:
两个磷原子______,铝离子______,硫元素的最高正价氧化物______。
(2)氯原子结构示意图如图 所示,X的数值为______。
所示,X的数值为______。
根据n的数值,可推断在化学变化过程中,氯原子容易______(填“失去”或“得到”)电子。
(3)观察数据表,请总结“七种元素”最高正价的规律是______。
【答案】2P Al3+ SO3 17 得到 元素的最高正价与最外层电子数相等
【解析】
(1)两个磷原子可以表示为2P,故填2P;每个铝离子带3个单位正电荷,可以表示为Al3+,故填Al3+;硫元素的最高正价是+6,氧元素化合价是-2,根据化合物中元素化合价代数和为零可知,硫元素的+6价氧化物化学式是SO3,故填SO3;
(2)氯原子核内质子数是17,故填17;根据氯原子结构示意图,X的数值是17,则 n=17-2-8=7,可推断在化学变化过程中,氯原子容易得到电子,故填得到;
(3)观察数据表,“七种元素”最高正价的规律是元素的最高正价与最外层电子数相等,故填元素的最高正价与最外层电子数相等。

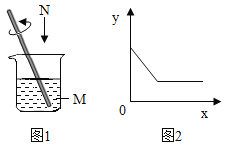
【题目】常温下,往盛放一定量M物质的烧杯中逐渐加入N物质并充分搅拌(如图1)。如图2横坐标x表示N物质的质量,纵坐标y表示烧杯中的某物理量(见下表)。下列实验与图2对应关系合理的是( )
M | N | Y | |
A | 硫酸铜溶液 | 铁粉 | 溶液的质量 |
B | 稀硫酸 | 锌粒 | 硫酸锌的质量 |
C | 稀盐酸 | 镁条 | 氢气的质量 |
D | 石灰水 | 二氧化碳 | 沉淀的质量 |
A. A B. B C. C D. D
【题目】某兴趣小组通过镁与稀盐酸反应探究影响反应速率的因素(镁的质量相等,镁条的形状一样,稀盐酸均过量),设计实验如表:
实验编号 | 盐酸的质量分数 | 镁的形态 | 溶液初始温度/℃ |
① | 3% | 粉末 | 30 |
② | 3% | 条状 | 20 |
③ | 6% | 粉末 | 20 |
④ | 6% | 条状 | 20 |
(1)镁与稀盐酸反应的化学方程式为______。
(2)若四组实验均以收集到250mL氢气为标准,要比较各组反应速率,则以上实验还需要测出的数据是______。
(3)实验______和______(填实验编号)是研究盐酸的浓度对该反应速率的影响。
(4)测定在不同时间产生的氢气的体积数据,绘制出图1,则实验②对应的曲线可能是______(填序号)。

(5)利用图2压力传感器进行实验,得到图3锥形瓶内的压强随时间变化的曲线图,发现实验测得的实际值比理论值偏大。请分析可能的原因______。
【题目】某实验小组用3克氯酸钾和二氧化锰混合物进行实验,加热该混合物t1时间后(杂质不反应),冷却,称量剩余固体的质量,重复以上操作,依次加热t2、t3、t4时间后测得剩余固体的质量,记录数据如下表:
加热时间 | t1 | t2 | t3 | t4 |
剩余固体质量(g) | 2.68 | 2.36 | 2.04 | 2.04 |
(1)加热t3时间后氯酸钾是否分解完全?_________(填“是”或“否”)
(2)完全反应后产生氧气的质量为_____________克;
(3)该混合物中氯酸钾的质量为_____?