题目内容
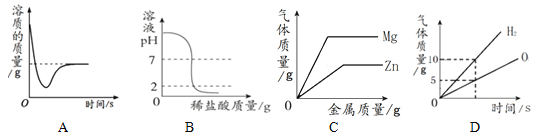
【题目】已知M、N分别是稀硫酸、氢氧化钠溶液中的一种。某化学兴趣小组同学在一定量的M中不断滴加N,并测定所得溶液的pH,如下图所示:
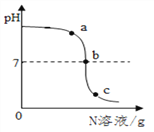
(1)M是______________。
(2)反应过程中,老师分别取图中a、b、c三处所对应的溶液,打乱顺序后,请同学们用一定的方法将三种溶液加以鉴别(不用测定溶液pH的方法)。
小明和小红分别取其中一种溶液进行实验:小明向所取溶液中加入___________溶液,观察到有蓝色沉淀生成。
结论:是a处溶液。
小红向少量另一种溶液中滴加酚酞溶液,观察到____________。
结论:是b处或c处溶液。
为进一步确定该溶液成分,小红又设计并完成如下实验:
实验步骤 | 实验现象 | 结论及化学方程式 |
取少量氧化铁,加入足量该溶液 | 固体完全溶解,且_____________ | 相关的化学方程式为_____________。 为c处溶液,并推知c处溶液中含有的离子有_____________(填写离子符号) |
结论:剩余一种为b处溶液。
【答案】 氢氧化钠溶液 硫酸铜 酚酞不变色 溶液变为黄色 3H2SO4 + Fe2O3 == Fe 2(SO4)3 + 3H2O H+ 、 Na+ 、 SO42-
【解析】(1)氢氧化钠溶液呈碱性,其pH大于7,硫酸溶液呈酸性,其pH小于7,由图象可以看出,开始时溶液的pH大于7,可以确定是向氢氧化钠溶液中滴加硫酸,氢氧化钠由显+1价的钠元素和显1价的氢氧根组成,根据化合价原则,其化学式为:NaOH;(2)氢氧化钠溶液和硫酸溶液发生中和反应生成硫酸钠和水,恰好完全反应时其pH等于7,氢氧化钠过量时显碱性,硫酸溶液过量时显酸性;由题意可知,反应后的溶液加入一种溶液生成了蓝色沉淀,蓝色沉淀是氢氧化铜,加入的溶液是可溶性的铜盐,例如:CuSO4或CuCl2或Cu(NO3)2等,可以推出原溶液有剩余的氢氧化钠,溶液应是a处溶液;根据结论:b处或c处的溶液,溶液的pH等于7和小于7,溶液呈中性和酸性,当加入无色酚酞试液时,酚酞不变色。由该溶液,向其中加少量的氧化铁,固体完全溶解,且溶液变为黄色,相关的化学方程式为:3H2SO4 + Fe2O3 == Fe 2(SO4)3 + 3H2O,可知酸过量,为c处溶液,并推知c处溶液中含有的离子有:H+ 、 Na+ 、 SO42-。

 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案