题目内容
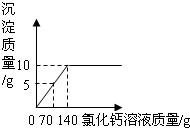 为了测定某纯碱样品中碳酸钠和氯化钠的含量(其他成分可忽略),将一定量的该样品溶解在100g水中,加入足量的氯化钙溶液,反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl,反应中物质间的质量关系如右图所示.当反应恰好完成时过滤,测得滤液中氯化钠的质量分数为6%.试计算该样品中:
为了测定某纯碱样品中碳酸钠和氯化钠的含量(其他成分可忽略),将一定量的该样品溶解在100g水中,加入足量的氯化钙溶液,反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl,反应中物质间的质量关系如右图所示.当反应恰好完成时过滤,测得滤液中氯化钠的质量分数为6%.试计算该样品中:
(1)氯化钠的质量;
(2)碳酸钠的质量分数.
解:
设:样品中碳酸钠的质量为x,原混合物中的氯化钠的质量为y,生成氯化钠的质量为z.
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100 117
x 10g z
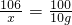
解得x=10.6g
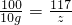
解得z=11.7g
 ×100%=6%
×100%=6%
解得y≈2.9g
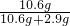 ×100%=78.5%
×100%=78.5%
答:样品中氯化钠的质量是2.9g;碳酸钠的质量分数是78.5%.
分析:(1)反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl及图示提供的数据求得氯化钠的质量;
(2)反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl及图示提供的数据求得碳酸钠的质量,进而求碳酸钠的质量分数.
点评:考查根据化学方程式的计算及溶液质量分数的计算.
设:样品中碳酸钠的质量为x,原混合物中的氯化钠的质量为y,生成氯化钠的质量为z.
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100 117
x 10g z
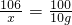
解得x=10.6g
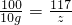
解得z=11.7g
 ×100%=6%
×100%=6%解得y≈2.9g
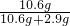 ×100%=78.5%
×100%=78.5%答:样品中氯化钠的质量是2.9g;碳酸钠的质量分数是78.5%.
分析:(1)反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl及图示提供的数据求得氯化钠的质量;
(2)反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl及图示提供的数据求得碳酸钠的质量,进而求碳酸钠的质量分数.
点评:考查根据化学方程式的计算及溶液质量分数的计算.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
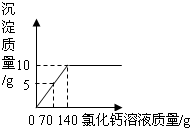 为了测定某纯碱样品中碳酸钠和氯化钠的含量(其他成分可忽略),将一定量的该样品溶解在100g水中,加入足量的氯化钙溶液,反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl,反应中物质间的质量关系如右图所示.当反应恰好完成时过滤,测得滤液中氯化钠的质量分数为6%.试计算该样品中:
为了测定某纯碱样品中碳酸钠和氯化钠的含量(其他成分可忽略),将一定量的该样品溶解在100g水中,加入足量的氯化钙溶液,反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl,反应中物质间的质量关系如右图所示.当反应恰好完成时过滤,测得滤液中氯化钠的质量分数为6%.试计算该样品中: 水是重要的资源,是人及一切生物生存所必需的,自然界的水含有各种杂质,很少能直接使用,须进行净化.
水是重要的资源,是人及一切生物生存所必需的,自然界的水含有各种杂质,很少能直接使用,须进行净化.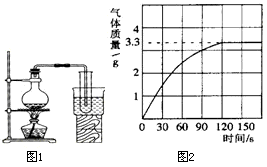 水是重要的资源,是人及一切生物生存所必需的,自然界的水含有各种杂质,很少能直接使用,须进行净化.
水是重要的资源,是人及一切生物生存所必需的,自然界的水含有各种杂质,很少能直接使用,须进行净化.