题目内容
【题目】下图为甲.乙、丙三种物质的溶解度曲线。
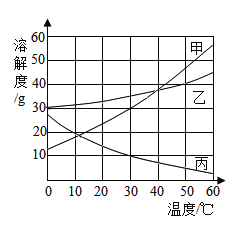
(1)20 °C时,三种物质中,溶解度最小的是_____;
(2)20° C时,将40g乙物质加入到50g水中,然后升温至50°C时,该溶液的溶质质量为_____;
(3)将50°C时等质量的甲、乙、丙的饱和溶液降温至10°C,此时三种溶液中溶质的质量关系为_____;(用“>、=”连接)。
【答案】丙 20g 乙>甲>丙
【解析】
(1)通过分析溶解度曲线可知,20℃时,三种物质中溶解度最小的是丙;
(2)20℃时,将40g乙物质加入到50g水中,然后升温至50℃,50℃时乙物质的溶解度是40g,根据溶解度概念可知,乙物质只能溶解20g,所以该溶液的溶质质量是20g;
(3)将50℃时甲、乙、丙三种物质的饱和溶液降温到10℃时,甲、乙的溶解度减小,丙的溶解度随温度的降低而增大,甲、乙有晶体析出,质量分数变小,溶液仍为饱和溶液,丙没有晶体析出,质量分数不变,一定温度下饱和溶液的溶质分数=![]() ,溶解度越大,质量分数越大,10℃时B的溶解度大于A的溶解度大于50℃时C的溶解度,所以10℃时三种物质的溶质质量分数由大到小的顺序是乙>甲>丙。
,溶解度越大,质量分数越大,10℃时B的溶解度大于A的溶解度大于50℃时C的溶解度,所以10℃时三种物质的溶质质量分数由大到小的顺序是乙>甲>丙。

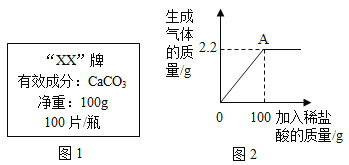
【题目】小滨同学为了测定某珍珠粉中碳酸钙的质量分数,称取12.5g珍珠粉样品,进行四次高温煅烧、冷却、称量剩余固体的重复操作(杂质不参加反应),记录数据如下:
操作次序 | 第一次 | 第二次 | 第三次 | 第四次 |
剩余固体质量/g | 10.8 | 9.6 | 8.1 | 8.1 |
试计算:
(1)完全反应后生成二氧化碳的质量为____________g;
(2)求该珍珠粉中碳酸钙的质量分数为____________。
【题目】做完“铁在氧气里燃烧”实验后,小明同学有两个疑惑不解的问题,于是他进行了以下探究活动,请你一同参与.
(问题)铁燃烧时溅落下来的黑色物质中还有没有铁呢?
(查阅资料)(1)自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO极易被氧化为Fe2O3)
(2)铁的氧化物均能溶于酸的溶液.
(实验探究)将冷却后的黑色物质碾碎,装入试管,加入 ______ 溶液,观察到的现象是 ______,说明铁燃烧时溅落下来的黑色物质中还含有铁.
(问题)铁燃烧的产物为什么不是 Fe2O3呢?
(查阅资料)
(1)Fe3O4和Fe2O3分解温度、铁的熔点见表:
Fe3O4 | Fe2O3 | 铁 | |
分解温度/℃ | 1538 | 1400 |
|
熔点/℃ |
|
| 1535 |
(2)Fe2O3高温时分解成Fe3O4
(理论探讨)根据实验现象,并结合表中数据,可推知铁在氧气里燃烧时产生的高温应在 ______ 之间,在此温度范围内Fe2O3已分解,所以铁在氧气里燃烧的产生是Fe3O4.
(拓展研究)
(1)实验中为了防止集气瓶炸裂,必须 ______.
(2)Fe2O3高温时会分解成Fe3O4和一种气体,请写出此反应的化学方程式 ______.
(3)有些超市的食品密封包装盒的透明盖内放有黑色的FeO粉末,若粉末的颜色______,就说明包装盒破损进气,这样售货员就能及时发现并处理.