题目内容
【题目】某热电厂用脱硫方法得到CaSO4生产K2SO4的工艺流程如下.
【资料】碳酸铵在水溶液中温度高于70℃时开始分解.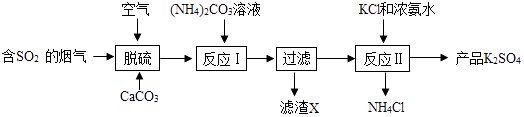
请回答下列问题:
(1)脱硫反应中的碳酸钙需要粉碎其目的是;
(2)脱硫过程的化学方程式为:2CaCO3+2SO2+O2+4H2O=2CaSO42H2O+2;
(3)反应Ⅰ的温度需要控制在60~70℃,其原因为;
A.60~70℃反应速率较快
B.高于70℃时碳酸铵分解,降低了原料的利用率
(4)滤渣X的化学式为;将NH4Cl溶液通过:、降温结晶、过滤、洗涤、干燥等操作步骤得副产物NH4Cl晶体;
(5)(NH4)2SO4与KCl溶液需在浓氨水中发生反应Ⅱ,析出K2SO4晶体,其中浓氨水的作用是;
(6)下列洗涤产品K2SO4晶体的方法中,你认为最好的方法是 .
A.常温时蒸馏水洗
B.冰水洗
C.饱和硫酸钾溶液洗.
【答案】
(1)增大反应物接触面积,加快反应速率
(2)CO2
(3)A,B
(4)CaCO3;蒸发浓缩
(5)降低K2SO4的溶解度,使K2SO4析出
(6)C
【解析】解:(1)脱硫反应中的碳酸钙需要粉碎其目的是增大反应物接触面积,加快反应速率.故填:增大反应物接触面积,加快反应速率.(2)由脱硫过程的化学方程式可知,反应前后都是2个钙原子,2个硫原子,8个氢原子,反应前是2个碳原子,反应后应该是2个碳原子,反应前是16个氧原子,反应后应该是16个氧原子,因此反应的化学方程式为:2CaCO3+2SO2+O2+4H2O=2CaSO42H2O+2CO2 . 故填:CO2 . (3)反应Ⅰ的温度需要控制在60~70℃,其原因是60~70℃反应速率较快,高于70同时能够防止碳酸铵分解.故选:AB.(4)滤渣X的化学式为CaCO3;
将NH4Cl溶液通过:蒸发浓缩、降温结晶、过滤、洗涤、干燥等操作步骤得副产物NH4Cl晶体.故填:CaCO3;蒸发浓缩.(5)(NH4)2SO4与KCl溶液需在浓氨水中发生反应Ⅱ,析出K2SO4晶体,其中浓氨水的作用是降低K2SO4的溶解度,使K2SO4析出.故填:降低K2SO4的溶解度,使K2SO4析出.(6)K2SO4晶体易溶于水,不溶于饱和硫酸钾溶液,因此下列洗涤产品K2SO4晶体的方法中,最好的方法是饱和硫酸钾溶液洗.故选:C.
【考点精析】本题主要考查了书写化学方程式、文字表达式、电离方程式的相关知识点,需要掌握注意:a、配平 b、条件 c、箭号才能正确解答此题.

 应用题作业本系列答案
应用题作业本系列答案【题目】化学就在我们身边,生活中蕴藏着丰富的化学知识.
(1)目前,人类以化石燃料为主要能源,化石燃料有煤、和天然气.
(2)液态二氧化碳灭火器可用于扑灭档案室发生的火灾,下列说法正确的(填序号).
A.液态二氧化碳气化后不会污染档案资料
B.二氧化碳可覆盖在燃烧物表面,隔绝空气
C.液态二氧化碳气化时吸热,降低了可燃物着火点
(3)氯化钠(NaCl) 和硝酸钾 (KNO3) 在不同温度时的溶解度及其溶解度曲线如图1:
温度(℃) | 10 | 20 | 40 | 60 | 80 |
KNO3 | 20.9 | 31.6 | 63.9 | 110 | 169 |
NaCl | 35.8 | 36 | 36.6 | 37.3 | 38.4 |
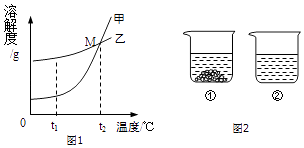
①图中能表示KNO3溶解度曲线的是(填“甲”或“乙”).
②t1oC时,等质量的甲和乙二种物质分别加水制成相应的饱和溶液,得到溶液质量较大的是 . (填“甲”或“乙”)
③20℃时,向两个分别盛有相同质量的硝酸钾和氯化钠的烧杯中,各加入100g水,充分溶解后,恢复至20℃,其结果如图2所示.下列有关说法中,正确的有 . (填字母编号)
A.烧杯①中溶解的是KNO3 , 烧杯②中溶解的是NaCl
B.烧杯②中溶液一定是不饱和溶液
C.升高温度或增加溶剂都有可能将烧杯①中固体全部溶解
D.若将烧杯①中的溶液变为不饱和溶液,溶液的溶质质量分数一定减小
(4)亚硝酸钠(NaNO2)是一种常用的防腐剂.结合图3“小资料”回答问题: 
①根据资料,小明设计如图的实验:
实验A中观察到的现象是 , 反应的化学方程式为 , 实验B观察到溶液最终变为色.
②亚硝酸钠加热分解放出有刺激性气味的气体,该气体可能是(填字母).
A.NO2 B.NH3 C.N2 D.SO2 .