题目内容
【题目】通过海水晾晒可得粗盐, 粗盐除NaCl外,还含有MgC12、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:
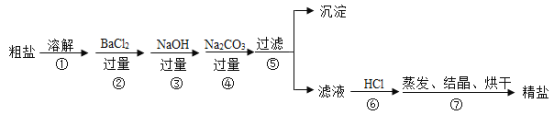
(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是_______________。
(2)第⑤步“过滤”操作中用到的仪器除烧杯、玻璃棒外还需要的玻璃仪器是_______________。得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、_______________(填化学式)。
(3)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH, 理由是_______________。
(4)在制备精盐的过程中,氯化钡和碳酸钠溶液的添加顺序是否可以颠倒________,理由是_______。
(5)在利用粗盐制备精盐过程的第⑥步操作中,加入适量盐酸的目的是_______________。
【答案】加快氯化钠的溶解速率 漏斗 CaCO3、BaCO3 会引入新的杂质氯化钾 不可以 碳酸钠的作用是既除去氯化钙,又除去过量的氯化钡 除去过量的氢氧化钠和碳酸钠
【解析】
(1)用玻璃棒搅拌,使粗盐与水充分接触,能加快氯化钠的溶解速率。故溶解时搅拌的作用是:加快氯化钠的溶解速率;
(2)过滤操作中用到的玻璃仪器有烧杯、玻璃棒、漏斗;第二步中过量的氯化钡和硫酸钠反应生成硫酸钡沉淀,第三步过量的氢氧化钠和氯化镁反应生成氢氧化镁沉淀,第四步加入过量的碳酸钠,除了和氯化钙反应生成碳酸钙沉淀外,还和第二步剩余的氯化钡反应生成碳酸钡沉淀,故第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、CaCO3、BaCO3;
(3)因为氢氧化钾会与氯化镁反应生成氢氧化镁沉淀和氯化钾,氯化钾对氯化钠来说就是新杂质,所以在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是:会引入新的杂质氯化钾;
(4)在制备精盐的过程中,氯化钡和碳酸钠溶液的添加顺序不可以颠倒,理由是:碳酸钠的作用是既除去氯化钙,又除去过量的氯化钡。如果顺序颠倒,过量的氯化钡不能被除去。
(5)最后得到的滤液中溶质除含有氯化钠外,还含有反应中剩余的碳酸钠和氢氧化钠,利用粗盐制备精盐过程的第⑥步操作,盐酸能和氢氧化钠、碳酸钠反应生成氯化钠,故加入适量盐酸的目的是:除去过量的氢氧化钠和碳酸钠。

 名校课堂系列答案
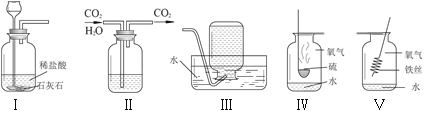
名校课堂系列答案【题目】请从A或B两题中任选1个作答,若两题均作答,按A计分。图中装置的夹持仪器已略去。
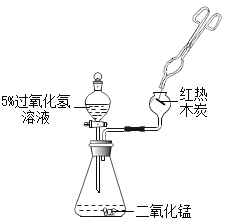
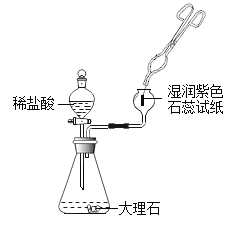
A用下图装置研究氧气 | B用下图装置研究二氧化碳 |
|
|
(1)滴入过氧化氢溶液后,锥形瓶中发生反应的化学方程式为____。 (2)木炭在氧气中燃烧时,现象是____。 | (1)滴入稀盐酸后,锥形瓶中发生反应的化学方程式为_____。 (2)石蕊试纸处的现象是_____。 |