题目内容
【题目】金属材料在生产、生活中有着广泛的应用。
(1)下列应用中使用金属材料的有_____(填字母)。
|
|
|
|
A、用金、银、铜等制作奖牌 | B、用化学纤维制作毛绒玩具 | C、用新型钢材建造“鸟巢” | D、用聚氯乙烯制造“水立方”外层膜 |
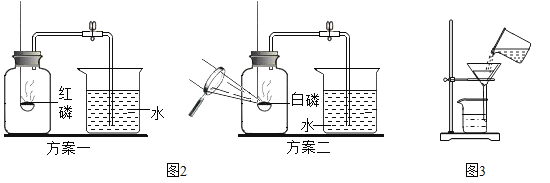
(2)化学小组为了验证铁、铜、镁、汞的金属活动性顺序,设计了如图实验方案:
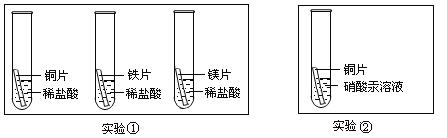
根据实验①判断出镁的金属活动性比铁强,依据的现象是_____,根据实验②的现象得出的结论是_____。
(3)向溶质为AgNO3、Cu(NO3)2、NaNO3的混合物溶液中,加入一定量的镁粉,充分反应后过滤,得到蓝色溶液,则所得蓝色溶液中一定含有的溶质是_____。
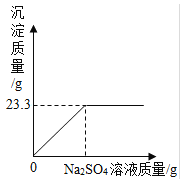
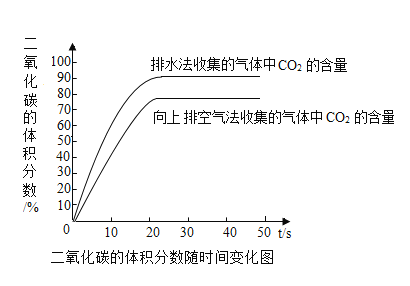
(4)为探究铁和锌两种金属与酸反应的状况,将等质量的两种金属分别与等质量的溶质质量分数相同的稀硫酸反应,产生氢气的质量与反应时间的函数关系如图所示。下列相关判断中,正确的是_____。
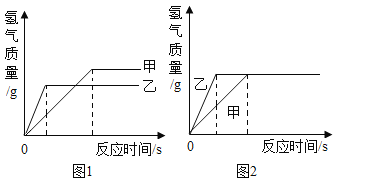
A 甲是锌,乙是铁
B 甲是铁,乙是锌
C 图1中消耗硫酸的质量甲>乙
D 图2中金属乙与硫酸充分反应后,金属乙一定有剩余
【答案】AC 镁片与盐酸反应产生气泡的速率比铁片快 铜的活动性比汞强 NaNO3、Mg(NO3)2,Cu(NO3)2 BC
【解析】
(1)金银铜牌和建造鸟巢用的新型金属都属于金属材料,故答案为:AC;
(2)根据实验①判断出镁的金属活动性比铁强,依据的现象是镁片与盐酸反应产生气泡的速率比铁片快;根据实验②的现象得出的结论是铜的活动性比汞强.故答案为:镁片与盐酸反应产生气泡的速率比铁片快;铜的活动性比汞强;
(3)向溶质为AgNO3、Cu(NO3)2、NaNO3的混合物溶液中,加入一定量的镁粉,镁不与硝酸钠反应,能与硝酸银和硝酸铜反应,充分反应后过滤,得到蓝色溶液,所得蓝色溶液中一定含有的溶质是NaNO3、Mg(NO3)2、Cu(NO3)2,可能含有硝酸银,故填:NaNO3、Mg(NO3)2、Cu(NO3)2。
(4)A.锌比铁活泼,和稀硫酸反应速率较快,反应需要时间短,最终铁和稀硫酸反应生成的氢气多,因此甲是铁,乙是锌,该选项说法错误;
B.甲是铁,乙是锌,该选项说法正确;
C.图1中,甲生成氢气的质量大于乙,消耗硫酸的质量甲>乙,该选项说法正确;
D.图 2中最终生成氢气质量相等,说明稀硫酸完全反应,铁一定有剩余,该选项说法不正确。
故填:BC。

 发散思维新课堂系列答案
发散思维新课堂系列答案