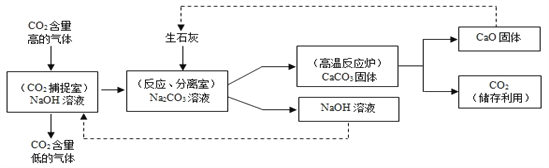
题目内容
【题目】某研究性学习小组的同学在学习铁及其化合物知识时进行了系列研究.
(1)下图为某兴趣小组探究铁生锈的三个实验,最先观察到铁锈的是_______(选填序号)。

(2)铁生锈的主要过程为:Fe![]() Fe(OH)2
Fe(OH)2![]() Fe(OH)3
Fe(OH)3![]() Fe2O3·xH2O;
Fe2O3·xH2O;
次要过程为:Fe![]() FeCO3。
FeCO3。
(3)铁锈组分的确定
某铁锈成分为Fe2O3·xH2O和FeCO3。为确定其组成,兴趣小组称取此铁锈样品25.4g,在科研人员的指导下用下图装置进行实验。
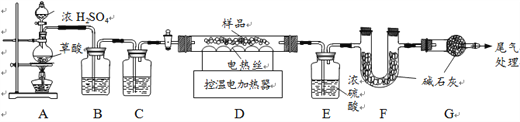
【查阅资料】Fe2O3·xH2O失去水分子温度为110℃,FeCO3在282℃分解为FeO和CO2。
温度高于400℃时铁的氧化物才能被CO还原。
①装置A中的反应为:H2C2O4 (草酸) ![]() CO↑+CO2↑+H2O。通过B、C装置可得到干燥、
CO↑+CO2↑+H2O。通过B、C装置可得到干燥、
纯净的CO气体,洗气瓶B中最好盛放________(选填序号)。
A.浓硫酸 B.澄清的石灰水 C.氢氧化钠溶液
②现控制D装置中的温度为300℃对铁锈进行热分解,直至D装置中剩余固体质量不再变化
为止,冷却后装置E增重3.6g,装置F增重2.2g。则样品中FeCO3的质量m(FeCO3)=______g,x=______。
(4)在钢铁厂的实验室,同学们了解到随着温度的升高,氧化铁在还原过程中能产生其他铁的氧化物,并最终被还原成铁。下图是某种热分析仪记录的CO与Fe2O3进行反应时的有关数据,并得到固体质量与反应温度的关系曲线.根据图象分析,固体质量由48.0g变为46.4g的过程中发生反应的化学方程式为___________________________。
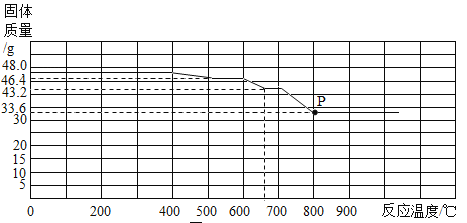
(5)同学们取了10g某菱铁矿样品(主要成分为FeCO3,杂质不参加反应),磨成粉末,加入200g足量稀硫酸,充分反应后称得剩余物的总质量为207.8g,计算该样品中FeCO3的质量分数。(要有完整的计算过程)已知:FeCO3+H2SO4====FeSO4+H2O+CO2↑_______________。
【答案】 C C 5.8 2 略 略
【解析】(1)铁是的条件是铁与水、氧气同时接触,其中氯化钠能加快铁的锈蚀,故最先观察到铁锈的是C;(3)①根据质量可知草酸与浓硫酸反应生成一氧化碳和二氧化碳,要得到纯净该做的一氧化碳,那么要将混合气体中的二氧化碳除去,由于澄清石灰水的浓度很低,吸收的二氧化碳的量很少,故用氢氧化钠溶液来除去二氧化碳,故选C;②浓硫酸能吸收水分,故E装置![]() 中增加的质量即为生成的水的质量;碱石灰吸收分解生成的二氧化碳,即F装置增加的质量即为FeCO3分解生成的CO2的质量。FeCO3在282℃分解为FeO和CO2,装置F增重2.2g,即生成的二氧化碳的质量为2.2g,利用化学方程式,根据FeCO3与二氧化碳反应的质量比可知FeCO3的质量为5.8g;铁锈样品的质量为25.4g,故Fe2O3·xH2O的质量=25.4g-5.8g=19.6g;装置E增重3.6g,即Fe2O3·xH2O分解生成的水的质量为3.6g,利用化学方程式,可计算出x=2 ;(4)固体质量由48.0g变为46.4g时,对应的温度是400-500℃,此时氧化铁与一氧化碳反应,根据氧化性氧化铁>四氧化三铁>氧化亚铁可知,与一氧化碳发生反应时,失去氧的质量=48.0g-46.4g=1.6g;氧化铁中氧元素的质量=48g
中增加的质量即为生成的水的质量;碱石灰吸收分解生成的二氧化碳,即F装置增加的质量即为FeCO3分解生成的CO2的质量。FeCO3在282℃分解为FeO和CO2,装置F增重2.2g,即生成的二氧化碳的质量为2.2g,利用化学方程式,根据FeCO3与二氧化碳反应的质量比可知FeCO3的质量为5.8g;铁锈样品的质量为25.4g,故Fe2O3·xH2O的质量=25.4g-5.8g=19.6g;装置E增重3.6g,即Fe2O3·xH2O分解生成的水的质量为3.6g,利用化学方程式,可计算出x=2 ;(4)固体质量由48.0g变为46.4g时,对应的温度是400-500℃,此时氧化铁与一氧化碳反应,根据氧化性氧化铁>四氧化三铁>氧化亚铁可知,与一氧化碳发生反应时,失去氧的质量=48.0g-46.4g=1.6g;氧化铁中氧元素的质量=48g![]() 14.4g,铁元素的质量=48g-14.4g=33.6g;残余固体中氧元素的质量=14.4g-1.6g=12.8g;铁氧原子的个数比=
14.4g,铁元素的质量=48g-14.4g=33.6g;残余固体中氧元素的质量=14.4g-1.6g=12.8g;铁氧原子的个数比=![]() =3:4,所以此时的还原产物是四氧化三铁,故反应的化学方程式表示为:Fe2O3+3CO
=3:4,所以此时的还原产物是四氧化三铁,故反应的化学方程式表示为:Fe2O3+3CO![]() 2Fe+3CO2;(5)由反应的化学方程式FeCO3+H2SO4====FeSO4+H2O+CO2↑,该反应生成了二氧化碳,二氧化碳会逸散到空气中,故减少的质量即为生成的二氧化碳的质量,利用化学方程式,根据二氧化碳与碳酸亚铁的质量比即可计算出碳酸亚铁的质量。
2Fe+3CO2;(5)由反应的化学方程式FeCO3+H2SO4====FeSO4+H2O+CO2↑,该反应生成了二氧化碳,二氧化碳会逸散到空气中,故减少的质量即为生成的二氧化碳的质量,利用化学方程式,根据二氧化碳与碳酸亚铁的质量比即可计算出碳酸亚铁的质量。
生成的二氧化碳的质量=10g+200g-207.8g=2.2g;
设碳酸亚铁的质量为x;
FeCO3+H2SO4====FeSO4+H2O+CO2↑
116 44
X 2.2g
![]() x=5.8g
x=5.8g
该样品中FeCO3的质量分数=![]() =58%
=58%

 一线名师提优试卷系列答案
一线名师提优试卷系列答案【题目】某兴趣小组同学对NaOH、Na2CO3、NaHCO3、NaCl等常见的钠的化合物进行了研究。
【知识回顾】下列相关说法正确的是___。
A.NaCl主要存在于海水中
B.烧碱(NaOH)和纯碱(Na2CO3)都属于碱
C.Na2CO3和NaHCO3的俗名分别为苏打和小苏打
D.NaOH和Na2CO3都可用于治疗胃酸过多
【分析判断】电解饱和食盐水可制得“84”消毒液。你认为“84”消毒液的有效成分可能是__。
A.SO2 B. Na2CO3 C.KMnO4 D.NaClO
【提出问题】NaOH露置于空气中易变质,那么实验室中的氢氧化钠有没有变质呢?该小组同学对实验室中一瓶氢氧化钠固体样品的成分进行了探究。
【查阅资料】①NaOH在空气中不会转化成NaHCO3。
②BaCl2溶液呈中性,Ba(OH)2是可溶性碱。
③CO2在饱和的NaHCO3溶液中几乎不溶解。
【提出猜想】猜想Ⅰ:样品中只有NaOH
猜想Ⅱ:样品中只有Na2CO3
猜想Ⅲ:样品中既有NaOH又有Na2CO3
【实验探究】兴趣小组同学设计如下实验进行探究。
实验操作 | 实验现象与结论 |
1.取少量样品,加足量水。 | 样品全部溶解,得无色溶液。 |
2.取少量实验1所得无色溶液于试管中,滴加足量稀盐酸。 | 有气泡产生,则猜想_______(填“Ⅰ”、“Ⅱ”或“Ⅲ”)不成立。 |
3.取少量实验1所得无色溶液于试管中, 滴加足量BaCl2溶液。 | 有白色沉淀产生,有关化学方程式为_____________。 |
4.实验操作:__________________。 | 对应现象:______________,则猜想Ⅲ成立。 |
【定量研究】上述样品变质的程度如何呢?该兴趣小组同学设计如下图 装置测定样品中Na2CO3的质量分数。

步骤如下:①按图连接好装置,并检查气密性;②准确称取该样品1.0g,放入烧瓶内;③打开分液漏斗活塞,滴加30.0%的稀硫酸至过量,关闭活塞;④反应结束后,量筒内液体的读数为55.0mL。(已知:室温条件下,CO2的密度为1.6gL﹣1)
(1)B装置集气瓶内原有的空气对实验结果_______________(填“有”或“没有”)影响。若用水代替饱和NaHCO3溶液,则所测CO2体积会偏小,原因是___________
(2)若将分液漏斗中的稀硫酸换成稀盐酸,则测试的结果可能______(填“偏大”、“偏小”或“不变”)。
(3)计算该样品中Na2CO3的质量分数((写出计算过程,结果保留到0.1%)__________。