��Ŀ����
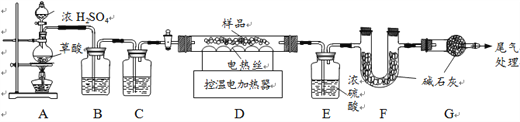
����Ŀ��A��B��C ��D��E��F�ֱ��������ֻ�����Ԫ����ɵij��������B������������㷺��һ������������п��������D�㷺���ڲ�������ֽ����֯��ϴ�Ӽ�������������θ���к���F���ɰ�������������֮���һ���ֹ�ϵ��ͼ��ʾ����ͼ�С� �� ����ʾ���˵������ܷ�����ѧ��Ӧ���� ������ʾ���ʼ����ת����ϵ�����ַ�Ӧ�������������ȥ����ش��������⣺

��1��B���ʵĻ�ѧʽΪ____________��F���ʵĻ�ѧʽΪ____________��
��2��D �� E��Ӧ�Ļ�ѧ��Ӧ����ʽΪ ________________________��
��3��A �� C��Ӧ�Ļ�ѧ��Ӧ����ʽΪ ________________________��
���𰸡� H2O HCl Na2CO3��Ca(OH)2��CaCO3����2NaOH���������ɣ� CaO + H2O��Ca(OH)2���������ɣ�
��������B������������㷺��һ������������п����������B��H2O��D�㷺���ڲ�������ֽ����֯��ϴ�Ӽ�����������D��Na2CO3������θ���к���F���ɰ�����������F��HCl ����D��E��F�֮��ķ�Ӧ��ת����ϵ��֪EΪNaOH����B��C֮����ת������C��ת��ΪE��C����D��Ӧ���Ʋ�C��Ca(OH)2����A��ת��ΪC����C��CaO��
��1��B���ʵĻ�ѧʽΪH2O��F���ʵĻ�ѧʽΪHCl��
��2��D �� E��Ӧ�Ļ�ѧ��Ӧ����ʽΪNa2CO3��Ca(OH)2��CaCO3����2NaOH
��3��A �� C��Ӧ�Ļ�ѧ��Ӧ����ʽΪCaO + H2O��Ca(OH)2

 ������ϰ�ο����뵥Ԫ���ϵ�д�
������ϰ�ο����뵥Ԫ���ϵ�д�