题目内容
【题目】以石灰石为原料制取高纯CaCO3的流程如图所示(杂质不溶于水也不与水反应):
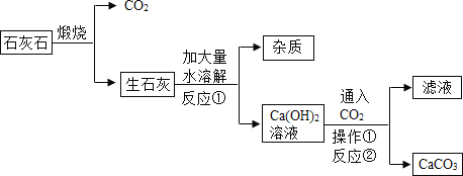
(1)操作1的名称______,该操作中所需要的玻璃仪器有烧杯、玻璃棒、______。
(2)写出反应①的化学方程式______,该反应属于______反应(填“放热”或“吸热”)
(3)检验Ca(OH)2是否完全转化为CaCO3的方法是______。
【答案】过滤 漏斗 CaO+H2O=Ca(OH)2 放热 取少量滤液于试管中,滴加几滴无色酚酞溶液,若无色酚酞溶液不变红色,则Ca(OH)2已完全转化为CaCO3
【解析】
(1)操作1得到了滤液和不溶性物质碳酸钙,所以为分离固体和液体的操作,为过滤,该操作中所需要的玻璃仪器有烧杯、玻璃棒、漏斗。
(2)反应①是氧化钙和水反应生成氢氧化钙,对应的化学方程式CaO+H2O=Ca(OH)2,该反应属于放热反应。
(3)检验Ca(OH)2是否完全转化为CaCO3的,就是检验氢氧化钙是否剩余,由于碳酸钙不溶,而氢氧化钙可溶且溶液为碱性,所以方法是取少量滤液于试管中,滴加几滴无色酚酞溶液,若无色酚酞溶液不变红色,则Ca(OH)2已完全转化为CaCO3。

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目