��Ŀ����
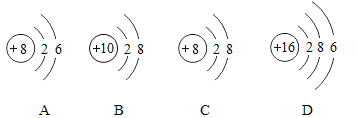
����Ŀ��ͼ1��ij��ȤС����ѧϰ�������ʱ���е�̽�������Ҫ��ش�������

��1��ͨ������ʵ��һ��֪���������ƻ����տ����е�________��
��2��ʵ����й۲쵽3������ƿ���ij̶�ΪA��B��C����֤��CO2����NaOH��Ca(OH)2��Ӧ������Cƿ��ʵ������ _________������
��3���������������˽��Ba(OH)2��Һ�еμӻ�ͨ������ͼ2�����ʻ������������A����Һ�Ժ�ɫ��B��C��D�о�������ɫ������
��д��D�Թ��з�Ӧ�Ļ�ѧ����ʽ _________��
�ڲ�ͬ�ļ���Һ�ж�����OH�������ԣ�����һЩ���ƵĻ�ѧ���ʣ���������Ba(OH)2���ʵ�ʵ�鲻�����ּ���������ʵ��� _________������ĸ��ţ�
��4���������ֹ�ҵ��ʹ�õ��������ƹ����ǩ��ͼ3��ʾ�����Ƕ����������ʽ�����̽����
��������⡿ _________
��������롿
����I���������Ͽ�֪����ҵ���������ƿ��ܺ���NaCl��
�����ҵ���������ƿ��ܺ���Na2CO3��ԭ���� _________���ü������ֱ�������
������ʵ�顿
ʵ�鲽�� | ʵ������ | ���ͻ���� |
��ȡ����������Ʒ���Թ��У���ˮ�ܽ� | ����ȫ���ܽ� | / |
�����������Һ�еμӹ����� _________ | һ��ʼ�����Ա仯��һ����������ʹ����ʯ��ˮ����ǵ����� | ��Ʒ�к���Na2C03 |
�����������Һ�еμӼ�����������Һ | ������ɫ���� | ��Ʒ�л�����NaCl����Ӧ�Ļ�ѧ����ʽΪ _________ |
���𰸡���1��ˮ����2���Աȣ���3����Ba(OH)2+SO2�TBaSO3��+H2O����C��
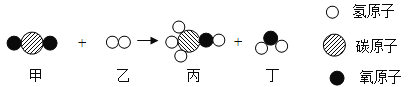
��4����������⡿�������ƺ���ʲô���ʣ�
��������롿��������������еĶ�����̼��Ӧ����̼������
������ʵ�顿�������NaCl+AgNO3=AgCl��+NaNO3��
��������
�����������1������ͼʵ��һ��֪���������ƻ����տ����� H2O�����Ҫ�ܷⱣ������2��ʵ�����пɹ۲쵽����������ƿ���ij̶ȴ�СΪA��B��C���Ա�Aƿ��Bƿ�� Cƿ��ʵ�������֤��CO2����NaOH��Ca(OH)2������Ӧ����3����D�Թ��еķ�Ӧ�Ƕ�������������������Ӧ����ѧ����ʽBa(OH)2+ SO2�TBaSO3��+H2O���ڸ��ݼ��ͨ�ԣ�����Ժ�ָʾ����Ӧ�����Ժ��ᷴӦ��������ǽ��������ﷴӦ�����Բ������ּ���������ʵ���C����4����������⡿�������ƺ���ʲô���ʣ���������롿��Ϊ��������������еĶ�����̼��Ӧ����̼���ƣ����Կ��ܺ���̼���ƣ�������ʵ�顿�ڸ����ܺ�̼���Ʒ�Ӧ������ʹ����ʯ��ˮ����ǵ����壬˵����������ᣬ����Ҫ�ų����������ӵĸ��ţ�����ֻ�ܵμ�������Ȼ��ƺ���������Ӧ����ѧ����ʽ��NaCl+AgNO3=AgCl��+NaNO3��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ����ѧ�仯�ı��������������������ɣ���ѧ�仯�е�һЩ���������������ж������Ƿ����˻�ѧ�仯��
����һ����ѧ�仯�е�����
ʵ������ | ʵ������ | ʵ����� |
��1�� | �����⣬�������� | ȼ����_______�ľ��ҵĻ�ѧ��Ӧ |
��2�� | þ����_______ͭ�����Ա仯 | þ��ϡ���ᷴӦ��ͭ����ϡ���ᷴӦ |
��3�� | ������ɫ���� | �÷�Ӧ�Ļ�ѧ����ʽ _____________ |
��4�� | �������ڵĹ����ɺ���ɫ��Ϊ_______ɫ | �����˻�ѧ�仯 |
���������������жϱ��ᣨH2C2O4����Һ������KMnO4��Һ������ѧ�仯��������ʲô�������ᾧ������ˮ�γ���ɫ��Һ������KMnO4��Һ��H2SO4��KMnO4�Ļ����Һ���������֪ʶ�����д��룺
��1�������ܲ��������������_________________________
��2�������ܲ��������������_________________________��
����Ŀ��ij��ѧС��������ϳ���̽������֪�����ȵ�����غ��Ȼ��ƵĻ�������ᴿ����ء���
�������ᴿ������
��һ�������£�20�棩�ܽ�Ⱥ��ܽ��ԵĹ�ϵ
�ܽ��S | S��10g | 1g��S��10g | 0.01g��S��1g | S��0.01g |
�ܽ��� | ���� | ���� | �� | ���� |
����������غ��Ȼ����ڲ�ͬ�¶�ʱ���ܽ��
�¶�/�� | 0 | 20 | 40 | 60 | 80 | 100 | |
�ܽ��/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
��1�������£�KNO3��NaCl���ܽ��Ծ�Ϊ
��2�����ݱ������ݣ�����KNO3�ܽ�����ߣ�
��3������KNO3���ܽ�����ߣ����KNO3��70��ʱ���ܽ��ԼΪ g��
������ᴿ���衿
��1��ѡȡ��Ʒ��95gKNO3��5gNaCl�Ļ���
��2������80��ʱKNO3�ı�����Һ����ˮԼ56.2mL��ˮ���ܶ�ԼΪ1gmL��1��
��3��������20��
��4���õ�����
������ᴿ������
Ϊ��֤����4���еõ��ľ���Ϊ������KNO3����С��ͬѧ�������֪ʶ���������ϳ�����������·������������Dz�ͬ���ʶ��ܽ�ȵ��Ӱ�켰ʵ�������ˮ���������ʧ��Ӱ�����أ�
����һ ͨ����ѧʵ����м��飬ȡ������4���еõ��ľ������Թ��У���ˮ�����Һ���μ� ���۲�ʵ������
������ ��������KNO3���������ԼΪ g����ȷ��0.1g���루4���еõ�������������бȽ�
������ ��95%���бȽϣ�
������ ��