题目内容
【题目】实验室有两瓶失去标签的无色溶液分别是Ba(OH)2溶液和稀硫酸,为完成鉴别设计如下方案,两种溶液分别标号为溶液A、溶液B。
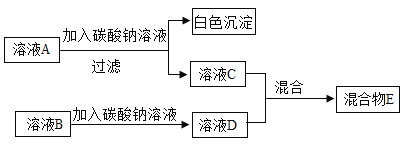
(1)溶液B中加入Na2CO3溶液的现象是___________。
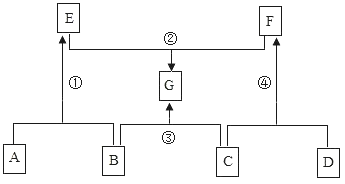
(2)溶液C和溶液D混合,可能有以下三种情况:
①若有气泡产生,写出反应的化学方程式___________。
②若有沉淀产生,通过现象可以推测溶液C的溶质是_____。
③若无明显现象,请分别列出混合物E中溶质的情况______。
【答案】有气泡产生 ![]() NaOH、Ba(OH)2或氢氧化钠、氢氧化钡 第一种情况:NaOH、Na2SO4;第二种情况:NaOH、Na2SO4、Na2CO3;第三种情况:Na2SO4;第四种情况:Na2SO4、H2SO4;第五种情况:Na2SO4、Na2CO3
NaOH、Ba(OH)2或氢氧化钠、氢氧化钡 第一种情况:NaOH、Na2SO4;第二种情况:NaOH、Na2SO4、Na2CO3;第三种情况:Na2SO4;第四种情况:Na2SO4、H2SO4;第五种情况:Na2SO4、Na2CO3
【解析】
(1)溶液A中加入Na2CO3溶液产生白色沉淀,则A是Ba(OH)2溶液,B是稀硫酸。稀硫酸中加入Na2CO3溶液,发生的反应是:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑,故反应现象是:有气泡产生。
(2)溶液C和溶液D混合,可能有以下三种情况:
①若有气泡产生,则溶液D中含有稀硫酸,溶液C中含有碳酸钠,反应的化学方程式为:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑。
②因为钠盐易溶于水,碳酸钡、硫酸钡都是白色沉淀,若有沉淀产生,则溶液C中有过量的氢氧化钡以及生成的氢氧化钠。
③若无明显现象,第一种情况:氢氧化钡与碳酸钠恰好反应,稀硫酸与碳酸钠恰好反应,E中溶质为NaOH、Na2SO4;第二种情况:碳酸钠有剩余,E中溶质为:NaOH、Na2SO4、Na2CO3;第三种情况:氢氧化钡与碳酸钠恰好反应生成的氢氧化钠被稀硫酸反应掉,稀硫酸与碳酸钠恰好反应,E中溶质为Na2SO4;第四种情况:氢氧化钡与碳酸钠恰好反应生成的氢氧化钠被稀硫酸反应掉,稀硫酸与碳酸钠反应时稀硫酸有剩余,Na2SO4、H2SO4;第五种情况:氢氧化钡与碳酸钠恰好反应生成的氢氧化钠被稀硫酸反应掉,稀硫酸与碳酸钠反应时碳酸钠有剩余,E中溶质为Na2SO4、Na2CO3。