题目内容
【题目】课外小组同学利用下图所示装置制取二氧化碳,并对其性质进行研究。A中盛有大理石,注射器中装有足量的稀盐酸,B中盛有浓硫酸(可吸收水蒸气),C中①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球。
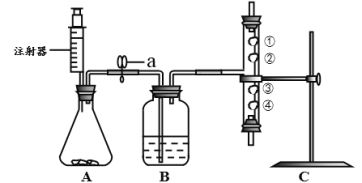
(1)检查装置气密性:打开a, 用手捂住A瓶外壁,若观察到B中导管口有气泡冒出,说明装置A_____(填“漏气”或“不漏气”)。
(2)C中能说明二氧化碳密度大于空气且能与水反应的现象是_______,二氧化碳与水反应的化学方程式为__________。
【答案】不漏气 ④比①先变红,②、③不变红 CO2+H2O=H2CO3
【解析】
(1)检查装置气密性:打开a,用手捂住A瓶外壁,若观察到B中导管口有气泡冒出,说明装置A不漏气;
(2)二氧化碳能与水反应生成了碳酸,碳酸能使紫色的石蕊变成红色;所以C中能说明二氧化碳密度大于空气且能与水反应的现象是 ④比①先变红,②、③不变红,二氧化碳与水反应的化学方程式为CO2+H2O=H2CO3。

 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案【题目】根据如表回答问题
温度(℃) | 20 | 40 | 50 | 60 | 80 | |
溶解度 (g/100g水) | NaCl | 36.0 | 36.6 | 37.0 | 37.3 | 38.4 |
NH4Cl | 37.2 | 45.8 | 50.4 | 55.2 | 65.6 | |
KNO3 | 31.6 | 63.9 | 85.5 | 110 | 169 | |
(1)40℃时,100g水中最多溶解NaCl______ g
(2)A是80℃含有120g水的KNO3溶液,经过如下操作,A经恒温蒸发得到B,B经降温至200C得到C,过滤后得到102gKNO3固体。流程如下图所示。
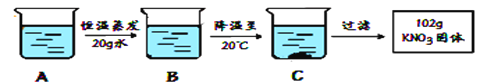
①A溶液为________(选填“饱和”或“不饱和”)溶液
②对以下过程的分析,正确的是_________(选填编号)
a.A到B的过程中,溶质质量没有改变 b.B中溶质与溶剂的质量比为169:100
c.A溶液的质量等于222g d.开始析出KNO3固体的温度在60℃至80℃之间