题目内容
【题目】兴趣小组发现,一 瓶久置空气中装有氧化钠固体的试剂瓶口有白色粉末。同学们对该白色粉末的成分进行了探究。
[猜想与假设]猜想I:白色粉末是碳酸钠
猜想II:白色粉末是氢氧化钠
猜想III:白色粉末是碳酸钠和氢氧化钠
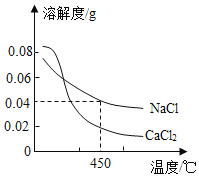
[查阅资料]氧化钠遇水迅速反应生成氢氧化钠: CaCl2溶液、 Ca(NO3)2溶液、BaCl2溶液都呈中性。
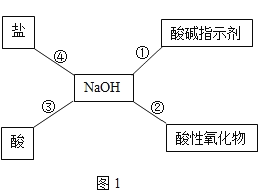
[实验探究]取少量白色粉末溶于水形成溶液A,设计如下实验:
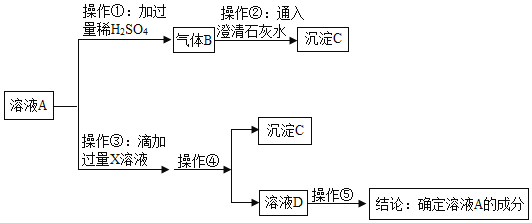
(1)由上述实验可知,猜想_____肯定不成立(填“Ⅰ”或“Ⅱ”或“Ⅲ”)。
(2)若操作①滴加过量稀硫酸有气体B产生,而滴加少量稀硫酸可能没有气体B产生。其可能的原因是_____(用化学方程式回答)。
(3)适合操作③的X溶液是_____(填字母序号)。
A CaCl2溶液
B Ca(OH)2溶液
C Ba(OH)2溶液
D Ca(NO3)2 溶液
(4)操作④用到的玻璃仪器除烧杯、玻璃棒外还需_____。
(5)请写出操作⑤的种实验方案并得出结论_____。
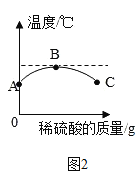
[拓展提升]某混合溶液中含有硫酸和盐酸,取该混合溶液20g于烧杯中,不断滴加氢氧化钡溶液,反应过程中烧杯中产生沉淀的质量、溶液pH的变化如图所示。求:
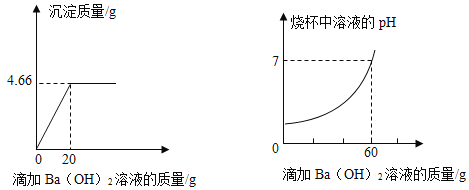
(6)氢氧化钡溶液中溶质的质量分数:_____。(写出计算过程,结果精确到0.1%)
(7) 20g混合溶液中HCl的质量为多少g。_____(写出计算过程,结果精确到0.01g)
【答案】II ![]() AD 漏斗 滴加酚酞试液,酚酞试液变红色,说明溶液A中含有氢氧化钠;或滴加氯化镁溶液,产生白色沉淀,说明溶液A中含有氢氧化钠(答一点,合理即可) 17.1% 2.92g
AD 漏斗 滴加酚酞试液,酚酞试液变红色,说明溶液A中含有氢氧化钠;或滴加氯化镁溶液,产生白色沉淀,说明溶液A中含有氢氧化钠(答一点,合理即可) 17.1% 2.92g
【解析】
根据氧化钠和水反应生成氢氧化钠,氢氧化钠和二氧化碳反应生成碳酸钠和水,和稀硫酸反应生成硫酸钠和水,和氯化镁反应生成白色沉淀氢氧化镁和氯化钠,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,和硝酸钙反应生成碳酸钙沉淀和硝酸钠,氢氧化钠溶液和碳酸钠溶液都是显碱性溶液,都能使酚酞试液变红色进行分析解答。
(1)由上述实验可知,加入稀硫酸时产生气体,说明溶液中含有碳酸钠,猜想Ⅱ肯定不成立;故填:II。
(2)若操作①滴加过量稀硫酸有气体B产生,而滴加少量稀硫酸可能没有气体B生成,其可能的原因是溶液中含有氢氧化钠,稀硫酸先和氢氧化钠反应生成硫酸钠和水,反应的化学方程式为:![]() ;故填:
;故填:![]() 。
。
(3)加入一种物质除去碳酸钠,但不能影响其他离子的检验,故适宜操作③的X溶液是氯化钙溶液或硝酸钙溶液;故填:AD。
(4)操作④是过滤,需要用到的玻璃仪器是烧杯、漏斗、玻璃棒;故填:漏斗。
(5)操作⑤是验证是否含有氢氧化钠,通常用酚酞溶液或硫酸铜溶液,因此,滴加酚酞试液,酚酞试液变红色,说明溶液A中含有氢氧化钠;或滴加氯化镁溶液,产生白色沉淀,说明溶液A中含有氢氧化钠(答一点,合理即可)。故填:滴加酚酞试液,酚酞试液变红色,说明溶液A中含有氢氧化钠;或滴加氯化镁溶液,产生白色沉淀,说明溶液A中含有氢氧化钠(答一点,合理即可)。
(6)设生成4.66g沉淀需要氢氧化钡的质量为x。
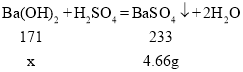
![]()
x=3.42g
氢氧化钡溶液中溶质的质量分数为:![]()
答:氢氧化钡溶液中溶质的质量分数为17.1%。
(7)设20g混合液中含氯化氢的质量为y。

![]()
y=2.92g
答:20g混合溶液中HCl的质量为2.92g。

【题目】2018年5月18日我国第一艘国产航母海试成功,航母的许多电子元件使用了黄铜。为测定某黄铜(假设合金中仅含铜和锌)中铜的质量分数,兴趣小组同学称取20g黄铜粉末于烧杯中,将80g稀硫酸分四次加入,充分反应,测得实验数据如下表所示:
第一次 | 第二次 | 第三次 | 第四次 | |
加入稀硫酸的质量(g) | 20 | 20 | 20 | 20 |
烧杯中剩余物的质量(g) | 39.92 | 59.84 | 79.80 | 99.80 |
(1)黄铜粉末完全反应生成氢气的总质量为__g。
(2)第三次实验后溶液中的溶质是___。
(3)该黄铜中铜的质量分数为多少__?(写 出计算过程)
【题目】实验室有一瓶碳酸钙和氯化钙粉末组成的均匀混合物,小科用相同溶质质量分数的稀盐酸和该混合物反应(所得溶液均为不饱和溶液)。四组实验数据记录如右表。请分析计算:
(1)反应后,稀盐酸还有剩余的是第______组。
(2)求混合物中碳酸钙和氯化钙质量之比。
(3)表中a的值为_____。
(4)求表中m的值。
实验组别 | 一 | 二 | 三 | 四 |
稀盐酸质量/g | 100.0 | 100.0 | 100.0 | 100.0 |
混合物质量/g' | 3.0 | 6.0 | 9.0 | 12.0 |
所得溶液质量/g | 101.9 | 103.8 | 105.0 | a |
剩余固体质量/ | 0 | 0 | m | n |