题目内容
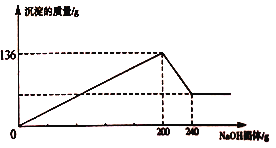
【题目】某材料只含金属镁和铝,课外小组为测定该材料中Mg的含量做了如下实验:取102g材料完全溶于盐酸得到溶液,将溶液分成两等份,向其中一份中逐渐加入NaOH固体,NaOH固体与溶液中产生沉淀的质量关系如下图所示,则该材料中Mg的质量分数为()[查阅资料: Al(OH)3 沉淀可以和NaOH反应生成无色溶液,反应的化学方程式为Al(OH)3 + NaOH= NaAlO2 + 2H2O]
A. 23.53% B. 42.65% C. 21.32% D. 47.06%
【答案】D
【解析】生成的氢氧化铝沉淀和氢氧化镁沉淀的质量是136g,当继续加入氢氧化钠时,氢氧化铝沉淀与氢氧化钠反应,沉淀的质量减少,故说明与氢氧化铝反应的氢氧化钠的质量为40g,设生成氢氧化镁的质量为x,则生成氢氧化铝的质量为136-x
Al(OH)3+NaOH=NaAlO2+2H2O
78 40
136-x 40
![]() =
=![]() ,解得x=58g
,解得x=58g
设参加反应的镁的质量为y
Mg-----Mg(OH)2
24 58
y 58g
![]() =
=![]() ,解得y=24g,
,解得y=24g,
样品中镁的质量分数为24÷(102÷2)×100%=47.06%,故选D。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
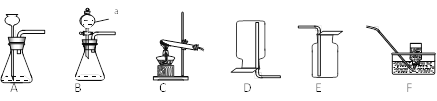
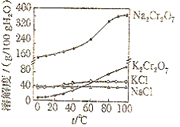
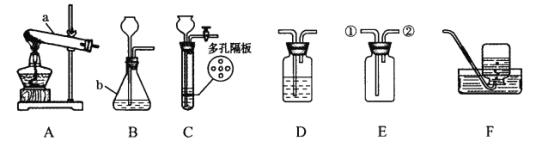
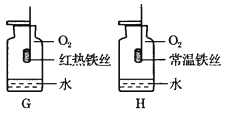
【题目】下列实验设计不能达到实验目的是( )
选项 | A | B | C | D |
实验目的 | 除去CO中的CO2,并回收CO | 探究可燃物燃烧所需的条件 | 除去氧化铜粉末中的铜粉 | 鉴别NH4NO3、CuSO4和NaCl三种白色粉末 |
实验设计 |
|
|
|
|
A. A B. B C. C D. D