题目内容
【题目】对稀硫酸的化学性质进行如下研究。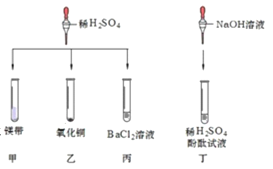
请回答下列问题:
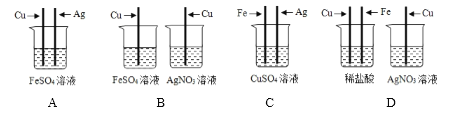
①甲中观察到的现象是_____ ,反应的化学方程式为_________ ; 乙中反应的现象是 __________;
丙中反应的化学方程式为_____;丁中溶液由无色变成红色。
②当甲、乙试管内的固体完全溶解后,将两试管内的物质混合并加入过量的锌片、过滤,则滤渣的成分 是_________,滤液中溶质的化学式为___________。
③请设计能说明 NaOH 与H2SO4是否恰好中和的实验方案。(本题中所用过的试剂不能再用)
_______ | 实验步骤 | 实验现象 | 实验结论 |
_________ | _________ | _________ |
④实验结束后,将乙(其中固体全部溶解)、丁两个实验的废液倒入同一个干净的废液缸中,静置,最终看到上层清液呈红色,废液下层有沉淀。由此推断上层清液的成分有酚酞、水和_____。 写出生成下层沉淀物的化学方程式_____________。
通过上述实验可知,进行化学实验研究,除需要考虑生成什么物质外,还需要考虑_______。
【答案】 镁带逐渐减小,冒气泡 Mg+H2SO4 =MgSO4 +H2↑ 黑色固体逐渐消失,溶液呈蓝色 BaCl2 +H2SO4 =BaSO4 ↓+2HCl Zn,Cu MgSO4,ZnSO4 酚酞 逐渐滴加氢氧化钠溶液,并不断震荡 溶液稍微变红 恰好中和 氯化钡 BaCl2 +Na2SO4=BaSO4+2NaCl 反应物是否过量
【解析】根据所学知识和题中信息知,①甲中观察到的现象是镁带逐渐减小,冒气泡,反应的化学方程式为Mg+H2SO4 =MgSO4 +H2↑;乙中反应的现象是黑色固体逐渐消失,溶液呈蓝色,氧化铜呈黑色,与硫酸反应生成硫酸铜,硫酸铜溶液呈蓝色;丙中反应的化学方程式为BaCl2 +H2SO4 =BaSO4 ↓+2HCl;丁中溶液由无色变成红色,酚酞试液遇碱变红。②当甲、乙试管内的固体完全溶解后,将两试管内的物质混合并加入过量的锌片、过滤,则滤渣的成分是Zn,Cu,锌片过量,锌片与硫酸铜反应置换出铜,锌比铜活泼,滤液中溶质的化学式为MgSO4,ZnSO4。③设计说明 NaOH 与 H2SO4 是否恰好中和。
酚酞 | 实验步骤 | 实验现象 | 实验结论 |
逐渐滴加氢氧化钠溶液,并不断震荡 | 溶液稍微变红 | 恰好中和,酚酞遇酸变红。 |
④实验结束后,将乙(其中固体全部溶解)、丁两个实验的废液倒入同一个干净的废液缸中,静置,最终看到上层清液呈红色,废液下层有沉淀。由此推断上层清液的成分有酚酞、水和氯化钡。生成下层沉淀物的化学方程式是BaCl2 +Na2SO4=BaSO4+2NaCl。进行化学实验研究,除需要考虑生成什么物质外,还需要考虑反应物是否过量。
点睛∶进行化学实验研究时,不仅要考虑反应物和生成物,反应条件,还要考虑到反应物是否过量等因素。酚酞试液遇酸不变色,与碱变红。

【题目】下表是从物质分类的角度认识部分酸碱盐的反应规律。
①请完成下表
序 列 | 物质分类的角度 | 实例 | 化学方程式 | |
反应物 | 生成物 | |||
1 | 盐和碱 | 盐和碱 | 碳酸钠和氢氧化钡 | Na2CO3+Ba(OH)2→BaCO3↓+2NaOH |
2 | 酸和金属 | 盐和氢气 | 铁和稀硫酸 | _______________ |
3 | 盐和盐 | 盐和盐 | 硝酸银和________ | ________________ |
4 | 盐和金属 | 盐和金属 | 锌和硫酸铜溶液 | __________________ |
②表中属于复分解反应的有__个;“锌和硫酸铜溶液”反应中现象是_____。
③可见,生成盐的途径有多种。当生成物中有硫酸钠时,可以是硫酸和氢氧化钠的反应,也可以是______和_____(写出具体物质的名称或化学式,酸和碱反应除外)。
④除了表中所列,盐还能与______(填物质类别名称)反应。
【题目】溶液在生产、生活中起着十分重要的作用。
(1)可作为溶质的是_______。
A.只有固体 B. 只有液体
C.只有气体 D. 气体、液体、固体都可以
(2)物质加入足量水中,能形成无色透明溶液的是_______。
A.汽油 B. 面粉 C. 纯碱 D. 硫酸铜
(3)物质加入水中形成溶液过程中,温度会升高的是_______。
A.烧碱 B. 氯化钠 D. 氧化钙 D. 碳酸钙
(4)下表是NaCl和KNO3在不同温度时的溶解度,回答问题。
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度g/100g水 | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | |
①两种物质中,溶解度受温度影响变化较大的是__________。
②NaCl和KNO3溶解度相等的温度范围是__________。
③KNO3晶体中含有少量NaCl,提纯KNO3晶体的方法是__________。
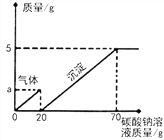
④60℃时,按图示操作:
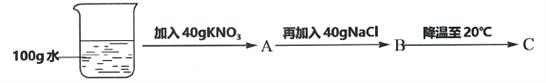
A中溶液是__________(填“饱和”或“不饱和”)溶液,C中溶液的总质量是__________g。
⑤50℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到50℃,剩余溶液的质量:NaCl溶液__________(填“大于”“等于”或“小于”)KNO3溶液。