题目内容
【题目】某混合物中含有碳酸钙和氯化钙,取该混合物6g,向其中加入一定质量的溶质质量分数为10%的稀盐酸,恰好完全反应,生成2.2gCO2。
计算:(1)所取混合物中碳酸钙的质量_____。
(2)反应后所得溶液中溶质质量分数_____。(结果精确到0.1%)
【答案】5g 16.3%
【解析】
碳酸钙和盐酸反应生成氯化钙和水,根据质量守恒定律,参加反应的反应物的总质量等于生成的生成物的总质量。
(1)设混合物中碳酸钙的质量为x
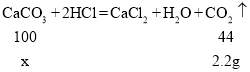
![]()
![]()
(2)设反应生成的氯化钙质量为y,盐酸中溶质氯化氢的质量为z
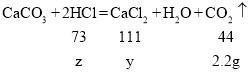

![]()
稀盐酸溶液的质量为![]()
反应后所得溶液中溶质质量为![]()
反应后所得溶液中溶质质量分数为![]()
答:所取混合物中碳酸钙的质量为5g,反应后所得溶液中溶质质量分数为为16.3%。

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案
相关题目