��Ŀ����
����Ŀ�����ֲ������Ϸ���CaCl2�������������������������ת����������CaCO3�Ƶ�CaCl2 �� ͼ�С�������ʾ��֮���ת����ϵ���������Ϸ�Ϊ��Ӧ��������뷴Ӧ����һ�����ʣ� ![]()
��ش��������⣺
��1��A�Ļ�ѧʽΪ����Ӧ�٢ڢ۶����漰�Ļ�����Ӧ��������Ӧ��
��2��ţţ��ΪCaCO3��һ����Ӧ�Ϳ���ת��ΪCaCl2 �� ��Ӧ�Ļ�ѧ����ʽΪ ��
��3���Ա���ͬѧ��ת����ϵ�����Ƿ��������������ʵĻ�ѧ���ʿ����Ż����ʵ�ת��;����д������B��һ��ת��ΪCaCO3�Ļ�ѧ����ʽ ��
���𰸡�
��1��CaO���û�
��2��CaCO3+2HCl�TCaCl2+H2O+CO2��
��3��Ca��OH��2+Na2CO3�TCaCO3��+2NaOH
���������⣺��1������ͼ���Ʋ�̼��Ƹ��·ֽ����������ƺͶ�����̼��Ϊ�ֽⷴӦ����������ˮ��Ӧ�����������ƣ�Ϊ���Ϸ�Ӧ������������ϡ���ᷴӦ�����Ȼ��ƺ�ˮ�Ͷ�����̼��Ϊ���ֽⷴӦ���� A�Ļ�ѧʽΪCaO����Ӧ�٢ڢ۶����漰�Ļ�����Ӧ�������û���Ӧ����2��CaCO3��һ����Ӧ�Ϳ���ת��ΪCaCl2 �� ̼��������ᷴӦ�����Ȼ��ơ�ˮ���Ͷ�����̼�����䷴Ӧ�Ļ�ѧ����ʽΪCaCO3+2HCl�TCaCl2+H2O+CO2������3������B��һ��ת��ΪCaCO3�Ļ�ѧ����ʽ����Ϊ��Ca��OH��2+Na2CO3�TCaCO3��+2NaOH��Ca��OH��2+CO2�TCaCO3��+H2O��
�ʴ�Ϊ����1��CaO�� �û�����2��CaCO3+2HCl�TCaCl2+H2O+CO2������3��Ca��OH��2+Na2CO3�TCaCO3��+2NaOH��Ca��OH��2+CO2�TCaCO3��+H2O��
����ͼ���Ʋ�̼��Ƹ��·ֽ����������ƺͶ�����̼����������ˮ��Ӧ�����������ƣ�����������ϡ���ᷴӦ�����Ȼ��ƺ�ˮ�Ͷ�����̼����������������̼���ƻ������̼��Ӧ����̼��ƣ����з�����

 ��Կ���Ծ�ϵ�д�
��Կ���Ծ�ϵ�д�����Ŀ������ʵ�鷽������������______��
ѡ�� | ʵ��Ŀ�� | �����Լ��� |
A | �����ͭ�ͻƽ� | �۲���ɫ |
B | ����ˮ����������Һ | ����������� |
C | ��ȥ������̼��������һ����̼ | ��ȼ |
D | ��ȥFeCl2��Һ�е�CuCl2 | ______________ |
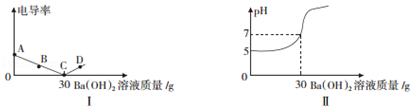
����Ŀ�����ʷ�����ѧ�仯��������һЩ����������Ҫ�������ָʾ�����ܹ۲쵽��ѧ�仯�������ǣ� ��
ʵ�����ͼʾ |
| | | |
ѡ�� | A | B | C | D |
A.A
B.B
C.C
D.D