题目内容
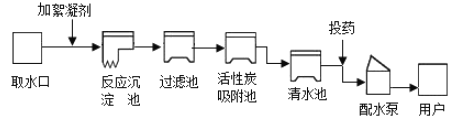
【题目】生物浸出技术在金属冶炼中应用广泛。嗜热细菌在 65~80℃酸性水溶液及氧气存在下,能氧化黄铜矿(主要成分CuFeS2 )产生硫酸盐,进而制取补血剂原料碳酸亚铁并回收铜。主要流程如图:
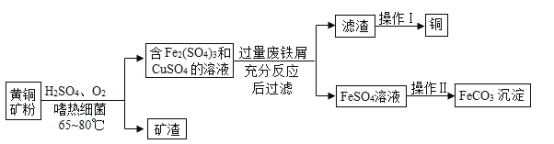
(1)黄铜矿的主要成分 CuFeS2中,Fe、Cu 的化合价均为+2,则 S 的化合价为_____。配平化学方程式:4CuFeS2+17O2+2H2SO4![]() xCuSO4+yFe2(SO4)3+zH2O,x、y、z 依次为_____。
xCuSO4+yFe2(SO4)3+zH2O,x、y、z 依次为_____。
(2)废铁屑与混合溶液发生的反应有:Fe+Fe2(SO4)3═3FeSO4,该反应所属基本类型是_____;另一反应的化学方程式是_____。
(3)操作Ⅰ包括:①过滤,②洗涤,③加足量稀硫酸,④干燥。正确的操作顺序是_____(填序号)。在实验室,过滤所用的玻璃仪器有_____。
(4)操作Ⅱ需加入一种试剂实现其转化,该试剂可以是_____(填化学式)。
(5)若所用废铁屑含有少量铁锈,对产品纯度有无影响?_____。
【答案】+2 4、2、2 化合反应; Fe+CuSO4═FeSO4+Cu ③①②④; 烧杯、玻璃棒、漏斗 Na2CO3 无影响
【解析】
(1)黄铜矿的主要成分 CuFeS2中,Fe、Cu 的化合价均为+2,根据化合物中元素化合价代数和为零可知,S的化合价为﹣2;配平化学方程式为:4CuFeS2+17O2+2H2SO4![]() 4CuSO4+2Fe2(SO4)3+2H2O。x、y、z 依次为4、2、2;
4CuSO4+2Fe2(SO4)3+2H2O。x、y、z 依次为4、2、2;
(2)废铁屑与混合溶液发生的反应有:Fe+Fe2(SO4)3═3FeSO4,该反应是由两种物质生成一种物质,属于化合反应;另一反应是铁和硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式是:Fe+CuSO4═FeSO4+Cu;
(3)滤渣中存在铜和铁,铁能与硫酸反应生成硫酸亚铁和氢气,铜不能与硫酸反应。操作顺序是首先加足量稀硫酸将铁转化为硫酸亚铁除去,再过滤,最后对滤渣洗涤、干燥,正确的操作顺序是③①②④;在实验室,过滤所用的玻璃仪器有烧杯、玻璃棒、漏斗;
(4)操作Ⅱ需加入一种试剂实现其转化,该试剂可以是碳酸钠,这是因为碳酸钠和硫酸亚铁反应生成碳酸亚铁沉淀和硫酸钠;
(5)若所用废铁屑含有少量铁锈,对产品无影响,这是因为铁锈不能和硫酸铁、硫酸铜反应,过滤存在于滤渣中,不影响铜的回收。