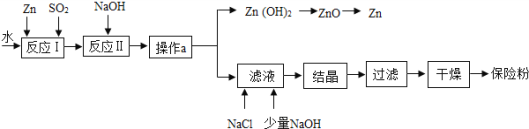
��Ŀ����
����Ŀ������ˮ����ˮ����ʾ��ͼ��ͼ����ش�
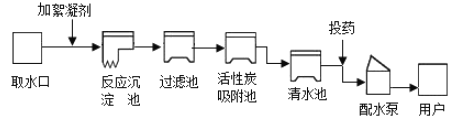
��1�����Գ�ȥˮ���ܽ��һЩ���ʺ���ζ���豸��_____������ĸ����
A ���˳� B ������ C ��ˮ��
��2�������������̣�������ѧ�仯����_____��
��3��������������ȡ������ˮ��Ӳˮ������ˮ������_____�����֣������п���ͨ��_____����ˮ��Ӳ�ȡ�
��4���ҹ��йز��Ź涨�����������̾���������û�������ˮ������0.3mgL��1����ͭ��1.0mg��L��1�����е�������ͭ��ָ����_____������ĸ����
A ԭ�� B ���� C Ԫ��
���𰸡�B Ͷҩ ����ˮ ��� C
��������
��1����ˮ�ľ��������У���Ȼ�������������������£�ˮ�еĽϴ�ġ��صIJ������³���������������ѧ������������������ˮ���γ���״���ʣ�ʹ���������ۼ������������˳������������ܳ�����С�������������̿���Գ�ȥˮ���ܽ��һЩ���ʺ���ζ���ʴ�Ϊ��B��
��2��Ͷҩ���������������������ʣ����ڻ�ѧ�仯���ʴ�Ϊ��Ͷҩ��
��3������Ӳˮ����ˮ�ķ����ǣ��÷���ˮ���������ˮ����ĭ�������ˮ����ĭ�ٵ���Ӳˮ��Ӳˮ�Ǻ������Ը�þ������϶��ˮ����п��Խ�Ӳˮ�еĸ�þ������ת���ɳ���������ˮ��Ӳ�ȣ��ʴ�Ϊ������ˮ����У�
��4����������Ԫ����ɵģ��ҹ��йز��Ź涨�����������̾���������û�������ˮ������0.3mgL��1����ͭ��1.0mg��L��1���������еġ�����ͭ��ָ����Ԫ�أ��ʴ�Ϊ��C��

����Ŀ��ij�������Ӫ���ɷֱ����(����̼ˮ��������Ҫָ���۵�)��
Ӫ���ɷֱ� |
��Ŀÿ100�� |
���� 1966ǧ�� ������ 7.5�� ֬�� 21.8�� ̼ˮ������ 60.7�� �� 2300���� |
(1)������������ָ_____(����ĸ���)��
A ����B ���� C Ԫ��D ����
(2)�÷������к���Ӫ������_____�֡�
(3)��������ʹ�õ�ʳ�ο����Ǽӵ��Σ�������ȱ����ܻ��еļ�����_____(������״���״�����������������)��
(4)������ͨ�����þ��������ϴ���װ�������������������ɫ��Ⱦ������������_____���ϡ�
(5)�й�������ʳָ�Ͻ���ÿ��ʳ��ʳ��ʯ����6�ˣ�����С��ij�����100�˸÷����棬�൱�ڳ���ʳ��_____�ˡ�(����С�����һλ)
����Ŀ��ͬѧ����Na2CO3��Һ��ŨHCl���о�����������ķ�Ӧԭ��ʱ���Է�Һ�ijɷֽ���̽����
���������裩�����������ʷ�����Ӧ�Ļ�ѧ����ʽΪ��_____���ɴ��Ʋ����Һ��һ����NaCl��������Na2CO3�����ᡣ
��ʵ��̽����
��1��ȷ����Һ���Ƿ������
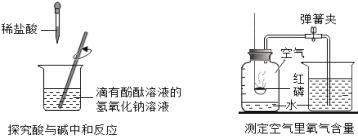
��ѡ���Լ�����������Ļ�ѧ���ʣ�ͬѧ��ѡ������ͼ����ʾ���������ʣ���������X�����ָʾ���е�_____��Һ��
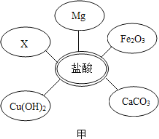
��ʵ����֤��ijͬѧ���Һ�м���������þ�ۣ��۲쵽_____��ȷ����Һ��һ��û�����ᡣ
��2��ȷ����Һ���Ƿ���Na2CO3��ijͬѧѡ��_____�����Һ��pH��l0��
ȷ����Һ��һ������Na2CO3��
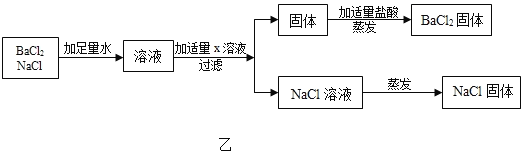
��3��������Һ���������ã����ӷ�Һ�еõ�������NaCl�����������ʵ�鷽����ơ�
���� | �����Լ� | ���뷽�� | �������� |
һ | ����Ca��NO3��2��Һ | ���ˡ������ᾧ | �����У������ǣ�_____ |
�� | �Թ�����_____ | _____ | ���� |
��4����չ���ã�
��ͼ�ҷ�������BaCl2��NaCl�Ĺ�������ʱ��X��Һ��������_____��