题目内容
【题目】(5分)在过氧化氢溶液的分解反应中,二氧化锰能作催化剂。
【提出问题】在过氧化氢溶液的分解反应中,除了二氧化锰,能否有其他物质也能作催化剂?
【查阅资料】在过氧化氢溶液的分解反应中,氧化铜也能作为催化剂
【进行实验】用天平称量0.2g氧化铜,取5mL5%过氧化氢溶液于试管中,进行如下实验:
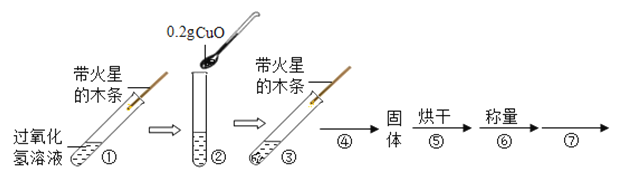
(1)填写下表
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
向步骤⑥得到的固体中再次加入过氧化氢,伸入带火星的木条, | 氧化铜也能作为过氧化氢分解的催化剂 |
(2)步骤①的目的 ;
(3)【拓展探究】设计如下四组实验,比较二氧化锰和氧化铜对过氧化氢溶液分解的催化作用,其中观察效果最差的____________
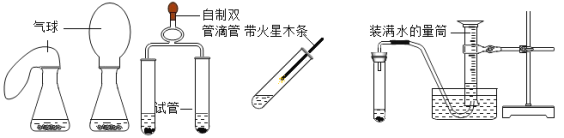
第一组 第二组 第三组 第四组
A.第一组同时实验,观察比较反应过程中两个气球体积的变化
B.第二组同时实验,观察比较反应过程中两个试管内产生气泡的快慢
C.第三组分两次实验,看木条是否能复燃
D.第四组分两次实验,比较收集一定体积的气体所需要的时间
【答案】(1)产生大量气泡、带火星的木条复燃 氧化铜质量仍为0.2克 产生大量气泡带火星的木条复燃 (2)对比 (3)C
【解析】
试题分析:(1)因为实验结论是氧化铜也能作为过氧化氢分解的催化剂,说明氧化铜能改变过氧化氢溶液的化学反应速率,故步骤③的现象是:产生大量气泡、带火星的木条复燃;催化剂不仅要能改变其他物质的化学反应速率,其本身的质量和化学性质还要不变,故步骤⑥是验证质量是否发生改变,故称量的结果是:氧化铜质量仍为0.2克;步骤⑦是验证氧化铜的化学性质是否发生改变,故现象为:产生大量气泡带火星的木条复燃
(2)步骤①的目的是:与步骤⑵作对比,看加入氧化铜前后的化学反应速率是否加快了
(3)A、第一组同时实验,观察比较反应过程中两个气球体积的变化,即气球膨胀速率的快慢,从而比较出反应的快慢,正确,B、第二组同时实验,可以直接观察比较反应过程中两个试管内产生气泡的快慢,从而比较出反应的快慢,正确,C、第三组分两次实验,看木条是否能复燃,但由于两个反应都会产生氧气,故木条都会复燃,故无法比较,错误,D、第四组分两次实验,比较收集一定体积的气体所需要的时间,所用时间越短,说明反应就越快,正确,故选C

【题目】(7分)小秋同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究。请填写下列空格
(1)取一支蜡烛,用小刀切下一小块,把它放入水中,蜡烛浮在水面上。结论:石蜡的密度比水__________;
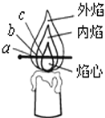
(2)点燃蜡烛,观察到火焰分为外焰、内焰、焰心三层。把一根火柴梗放在火焰中(如图)约1s后取出可以看到火柴梗的a处最先碳化。结论:蜡烛火焰的_________温度最高;
(3)再将一支干燥的烧杯罩在蜡烛火焰上方,烧杯内壁出现水雾。取下烧杯,迅速向烧杯内倒入少量澄清的石灰水,振荡。澄清石灰水变浑浊。结论:蜡烛燃烧以后的生成物是_____________和____________
(4)小蓓同学进一步对蜡烛燃烧产生火焰的原因产生了兴趣点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生(如图所示)。由此可知:蜡烛燃烧产生的火焰是由________(填“固态”或“气态”)物质燃烧形成的。

查阅资料
物质 | 熔点╱℃ | 沸点╱℃ | 燃烧时温度╱℃ |
石蜡 | 50∽70 | 300∽550 | 约600 |
铁 | 1535 | 2750 | 越1800 |
钠 | 97.8 | 883 | 越1400 |
由上表可知:物质燃烧能否产生火焰与其 (填“熔点”或“沸点”)和燃烧时温度有关。由此推测:钠在燃烧时, (填“有”或“没有”)火焰产生。
