题目内容
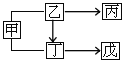
【题目】过氧化钙晶体(CaO28H2O)微溶于水,也不溶于乙醇,可溶于酸,可作分析试剂、医用防腐剂、消毒剂。以下是一种制备过氧化钙的实验流程:
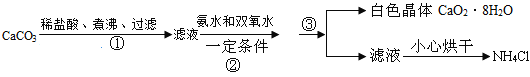
回答下列问题:
(1)过氧化钙(CaO2)中氧元素的化合价为______________。
(2)步骤①的具体操作为逐滴加入稀盐酸,至溶液中尚存有少量固体,将溶液煮沸,趁热过滤。发生的化学反应方程式为_______________;将溶液煮沸的目的是________________。
(3)步骤②中反应的生成物为_________________、______________。
(4)步骤③的操作名称是______________。
【答案】 -1 CaCO3+ 2HCl= CaCl2 +CO2↑+H2O 除去过量的稀盐酸 CaO2 NH4Cl 过滤
【解析】本题通过流程图考查了元素化合价的计算,盐酸的性质和过滤,读懂流程图是解题的关键。
(1)根据在化合物中正负化合价代数和为零,钙元素显+2,设:氧元素的化合价是x,可知CaO2中氧元素的化合价:(+2)+2x=0,则x=-1;
(2)步骤①的具体操作为逐滴加入稀盐酸,发生了碳酸钙与盐酸反应生成了氯化钙、水和二氧化碳,发生的化学反应方程式为CaCO3+ 2HCl= CaCl2 +CO2↑+H2O;将溶液煮沸的目的是除去过量的稀盐酸;
(3)根据流程图可知步骤②中反应的生成物为CaO2、NH4Cl;
(4)步骤③的操作是将固体和液体分开,所以操作名称是过滤。

练习册系列答案
相关题目