题目内容
【题目】在牙膏中常用轻质碳酸钙粉末作摩擦剂。小李在实验室以石灰石(杂质不反应也不溶于水)为原料制取轻质碳酸钙和氢氧化钠。
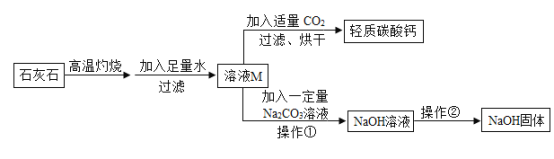
(1)操作②中需要使用到玻璃棒,其作用是_________。
(2)该流程中有两个反应,产物中均出现碳酸钙,这两个反应的化学方程式分别_____、___。
(3)为了验证加入Na2CO3溶液后,溶液M 中的溶质是否反应完全,可取上层清液加入___(填序号)进行检验。
A 碳酸钠溶液 B 铁粉 C 无色酚酞
【答案】防止局部温度过高,造成液滴飞溅 CO2+Ca(OH)2=CaCO3↓+H2O Na2CO3+Ca(OH)2=CaCO3↓+2NaOH A
【解析】
(1)操作②为蒸发结晶的操作,其中需要使用到玻璃棒,其作用是:防止局部温度过高,造成液滴飞溅。
(2)碳酸钙高温灼烧生成氧化钙和二氧化碳,氧化钙和水反应生成氢氧化钙,溶液M为氢氧化钙溶液。氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,这两个反应的化学方程式分别:CO2+Ca(OH)2=CaCO3↓+H2O、Na2CO3+Ca(OH)2=CaCO3↓+2NaOH。
(3)加入Na2CO3溶液后,生成了NaOH,则加入无色酚酞后无论氢氧化钙是否剩余都会使溶液变为红色,无法验证氢氧化钙是否完全反应,而铁粉不与反应物和生成物发生反应,则也不能用来验证;再加碳酸钠溶液,若有白色沉淀产生,说明氢氧化钙有剩余,若无现象,则氢氧化钙反应完全。故选:A。

练习册系列答案
相关题目