题目内容
【题目】某兴趣小组欲探究Zn、Cu、Ag、R四种金属的活动性顺序(R为未知金属),进行了如下实验:
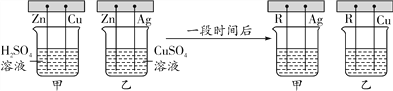
图A 图B
(1)如图A所示,将四根金属丝同时插入烧杯中,则乙中发生反应的化学方程式为_______。
(2)一段时间后,将烧杯中四根金属丝依次替换为R、Ag、R、Cu,如图B所示。
①若甲中出现气泡,乙中无明显现象,可得出Zn、Cu、Ag、R的活动性顺序由强到弱为______________;
②若甲中无明显现象,乙中R表面出现红色固体,则不能推出的结论是___(填字母代号)。
A. R<H B. R>Cu C. R>Zn D. R>Ag
【答案】 Zn+CuSO4=== ZnSO4+Cu Zn、R、Cu、Ag C
【解析】欲探究Zn、Cu、Ag、R四种金属的活动性顺序(R为未知金属),则由图可知:(1)如图A所示,将四根金属丝同时插入烧杯中,则乙中为锌和硫酸铜反应,发生反应的化学方程式为:Zn+CuSO4=ZnSO4+Cu;(2)一段时间后,将烧杯中四根金属丝依次替换为R、Ag、R、Cu,如图B可知:①根据“若甲中出现气泡,乙中无明显现象”,则推测:甲中R与硫酸溶液反应,而烧杯乙中R与溶液不反应,则可推测出:烧杯乙中的物质是 ZnSO4溶液,可得出Zn、Cu、Ag、R的活动性顺序由强到弱为:Zn>R>Cu>Ag;②第一种情况:根据“若甲中无明显现象,乙中R表面出现红色固体”,则可推测的结论为:“甲中R”与硫酸溶液可能反应,但较慢,不易察觉;也可能不反应,故d能推测出;“乙中R”与硫酸铜溶液反应,则可推测b.R>Cu和a.R>Ag,但题目中不能推测c.R>Zn。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目