题目内容
【题目】阅读下面科普短文。
氨(NH3)常用来制化肥和硝酸,但是科学家们发现它还是一种很有前景的燃料。
现有的化石燃料燃烧时,都会产生温室气体CO2,而氨燃烧时生成N2和H2O两种对环境友好的产物。氨价格低、制造技术成熟,便于普及使用。传统的工业合成氨是将氮气和氢气在20~50MPa的高压和500℃的高温条件下,用铁作催化剂合成的。
氨很容易液化,将氨常温下加压到1MPa,或者常压下温度降到-33℃,均可将其液化。而为了获得含有相同能量的液态氢(H2),常温下需要136MPa的压力来压缩它,显然超出了车载燃料储存的压力极限。
氨虽然有毒, 但氨具有强烈的刺激性气味,一旦发生泄漏,达到人们觉察到时浓度的1000倍才会致命,因此很容易被发现并及时补救。氨比空气轻, 泄漏后扩散快, 不会聚积。泄漏在大气中的氨还可以参与自然循环,随雨雪移动后,与其他物质反应或被植物吸收。
依据文章内容,回答下列问题。
(1)化石燃料燃烧都会生成CO2的原因是____________________。
(2)文中提到氨的物理性质有_______(答出一点)。
(3)从阅读材料中可以看出,将气体液化的途径有________。
(4)请写出氨燃烧生成N2和H2O的化学方程式________________________。
(5)德国化学家格哈德·埃特尔在固体表面化学的研究中取得了非凡的成就,其成果之一是揭示了氮气与氢气在催化剂表面合成氨的反应过程。下图为该过程的微观示意图(图中![]() 表示氮原子,
表示氮原子,![]() 表示氢原子,
表示氢原子,![]() 表示催化剂)。符合上述反应过程的顺序是_______(填字母序号)。
表示催化剂)。符合上述反应过程的顺序是_______(填字母序号)。
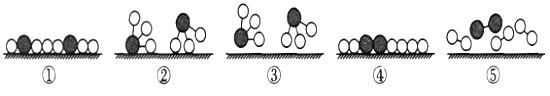
A. ⑤④①③② B. ④⑤①②③ C. ④⑤①③② D. ⑤④①②③
【答案】 都含碳元素 比空气氢、有刺激性气味(或易液化) 常温加压和常压降温 4NH3 + 3O2 ![]() 2N2 +6H2O D
2N2 +6H2O D
【解析】(1)根据化石燃料都含碳元素解答;(2)需要通过化学变化表现出来的性质,属于物质的化学性质,不需要通过化学变化表现出来的性质,属于物质的物理性质;(3)根据题中信息解答;(4)根据氨燃烧生成N2和H2O解答;(5)根据化学变化的实质分析解答。(1)根据质量守恒定律可知,化石燃料都会生成CO2的原因是都含有碳元素;(2)文中提到氨的物理性质有比空气氢、有刺激性气味(或易液化);(3)将气体液化的途径有常温加压和常压降温;(4)氨燃烧生成N2和H2O的化学方程式为4NH3+3O2点燃2N2+6H2O;(5)根据化学反应的实质为反应物分子中的原子彼此分开,重新组合成新分子的过程,可知反应过程的顺序是⑤④①②③,故选D。