题目内容
经检测某溶液中含有大量K+、H+、Cl-、NO-3离子.
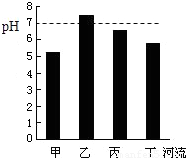
(1)若向溶液中滴入紫色石蕊溶液,该溶液应显 色,说明溶液pH 7(填“大于”“小于”或“等于”),若要配制该溶液,可以用盐酸和硝酸钾,也可以用 和
配制.
(2)若要除去溶液中的氯化物,而不引入其他杂质,宜加入适量试剂是
(1)小红;小于;KCl ;HNO3 (2)AgNO3[提示:溶液中含大量H+,显酸性,pH<7,使紫色石蕊溶液变红;这四种粒子既可形成
HCl和KNO3,也可形成KCI和HNO3.Ag+和CI-会生成AgCl沉淀]

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
 23、[2007年1月17日新华社消息]国家卫生部对《生活饮用水卫生标准》进行全面修订和完善.新标准为国家标准,对饮用水增加了亚硝酸盐、溴酸盐、贾第虫和隐孢子虫等危及人健康的有害物检测指标.新标准于2007年元月7日起强制执行.新标准水质指标将从以前的35项,增加到106项.这意味着今后居民饮用水有更多的检测项目把关.
23、[2007年1月17日新华社消息]国家卫生部对《生活饮用水卫生标准》进行全面修订和完善.新标准为国家标准,对饮用水增加了亚硝酸盐、溴酸盐、贾第虫和隐孢子虫等危及人健康的有害物检测指标.新标准于2007年元月7日起强制执行.新标准水质指标将从以前的35项,增加到106项.这意味着今后居民饮用水有更多的检测项目把关. 某制碱厂以岩盐水为主要原料生产纯碱(Na2CO3)和其他副产品.
某制碱厂以岩盐水为主要原料生产纯碱(Na2CO3)和其他副产品.
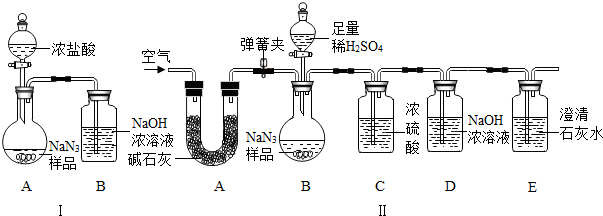

 装置。
装置。