题目内容
【题目】在古代,人们常用贝壳(主要成分是碳酸钙,杂质不参与反应且不溶于水)和纯碱为原材料制取烧碱,其制取流程如图:
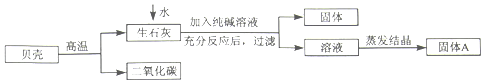
(1)写出加入纯碱溶液后发生反应的化学方程式: ;
(2)【问题与发现】固体A是纯净的氢氧化钠吗?
【猜想与假设】根据反应原理,同学们提出以下猜想:
甲的猜想:A是纯净的氢氧化钠固体.
乙的猜想:A是氢氧化钠和氢氧化钙的混合物.
你的猜想: .
【实验验证】
实验操作 | 现象 | 结论 | |
甲 | 取少量固体A,用适量水溶解后,滴加几滴无色酚酞溶液. | 溶液变红 | 猜想成立 |
乙 | 取少量固体A,用适量水溶解后,滴加几滴饱和碳酸钠溶液. | 猜想不成立 | |
你 | 猜想成立 |
【反思与评价】同学们讨论后,认为甲的结论不一定成立,原因是 .
【答案】
(1)CO2+Ca(OH)2=CaCO3↓+H2O;
(2)氢氧化钠和碳酸钠的混合物;没有出现白色沉淀;取少量固体A,溶于适量水形成溶液后,滴加足量的稀盐酸;有气泡产生;因为碳酸钠、氢氧化钙的水溶液都显碱性,它们都能够使酚酞试液变红色,所以酚酞试液变红色,不能说明是纯净的氢氧化钠
【解析】
试题分析:
(1)氢氧化钙与碳酸钠反应生成碳酸钙和氢氧化钠,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O.
(2)【猜想与假设】氧化钙和水反应生成了氢氧化钙,而氢氧化钙可以和碳酸钠反应生成氢氧化钠,若氢氧化钙是过量的,则在反应后的溶液中还含有氢氧化钙,若碳酸钠是过量的,则在反应后的溶液中还含有碳酸钠,即可以作出固体A为氢氧化钠和碳酸钠的猜想;【探究与验证】乙:取少量固体A,溶于适量水形成溶液后,滴加几滴饱和碳酸钠溶液,如果没有出现白色沉淀,说明氢氧化钠中不含氢氧化钙,猜想不成立.你:取少量固体A,溶于适量水形成溶液后,滴加足量的稀盐酸;如果有气泡产生,说明氢氧化钠中含有碳酸钠,猜想成立.【反思与评价】根据实验流程,可以判定甲同学设计的方案不严密,理由是:因为碳酸钠、氢氧化钙的水溶液都显碱性,无论碳酸钠过量还是氢氧化钙过量,混有碳酸钠或氢氧化钙的氢氧化钠配成溶液后,都能够使酚酞试液变红色,所以酚酞试液变红色,不能说明是纯净的氢氧化钠,故甲同学设计的方案是错误的;
故答案为:
(1)CO2+Ca(OH)2=CaCO3↓+H2O;
(2)氢氧化钠和碳酸钠的混合物;没有出现白色沉淀;取少量固体A,溶于适量水形成溶液后,滴加足量的稀盐酸;有气泡产生;因为碳酸钠、氢氧化钙的水溶液都显碱性,它们都能够使酚酞试液变红色,所以酚酞试液变红色,不能说明是纯净的氢氧化钠

 阅读快车系列答案
阅读快车系列答案