题目内容
【题目】根据如图所示的实验回答问题:
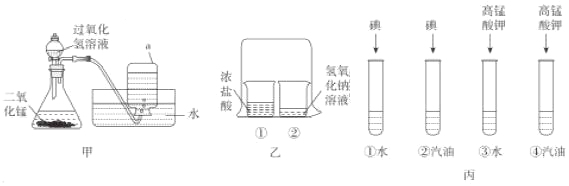
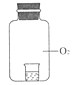
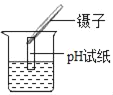
(1)甲实验中仪器a的名称是_____,此实验中二氧化锰起_____作用。
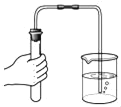
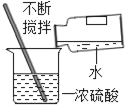
(2)乙实验在学习酸碱盐的化学性质时所做,在烧杯②中滴加2滴酚酞溶液后,扣上大烧杯。一段时间后看到的现象是_____,得出的结论是_____。
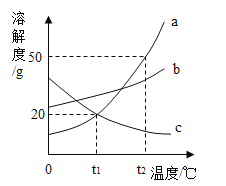
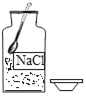
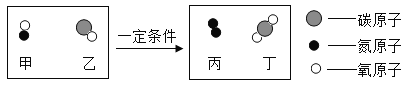
(3)丙实验是一组对比实验,通过试管_____(填序号)对比,可以比较不同溶质在相同溶剂中的溶解性。
【答案】集气瓶 催化 烧杯中红色溶液变成无色 分子是不断运动的 ①和③或②和④
【解析】
(1)甲实验中仪器a的名称是集气瓶;过氧化氢在二氧化锰的催化作用下分解为水和氧气,此反应中二氧化锰是催化剂,起到了催化作用;故填:集气瓶;催化;
(2)在实验乙的烧杯②中滴加2滴酚酞溶液后,扣上大烧杯,一段时间后看到的现象是②烧杯中红色溶液变成无色,是因为浓盐酸中的氯化氢分子是不断运动的,运动到氢氧化钠溶液中时,和氢氧化钠反应生成氯化钠和水,氢氧化钠完全反应或氯化氢过量后,溶液显中性或显酸性,溶液由红色变成无色,得出的结论是分子是不断运动的。
故填:②烧杯中红色溶液变成无色;分子是不断运动的;
(3)通过试管①和试管③可以比较碘和高锰酸钾在水中的溶解情况;通过试管②和试管④可以比较碘和高锰酸钾在汽油中的溶解情况,即比较不同溶质在相同溶剂中的溶解性;故填:①和③或②和④。

 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案【题目】现有25g石灰石样品,请按下面要求计算
(1)25g样品与足量的稀盐酸反应放出8.8gCO2(杂质不溶于酸,且不与酸反应),请计算该样品的纯度(CaCO3的质量分数)是多少?_____
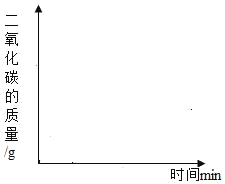
(2)若将25g样品平均分成两份,分别加工成块状和粉末状,将两份样品分别放入锥形瓶中,同时加入相同体积,相同浓度的足量稀盐酸充分反应,请在图象上画出块状样品与稀盐酸反应放出CO2的曲线示意图。_____
(3)若将一定质量的该石灰石样品高温煅烧,有关物质质量反应时间的变化如表所示:
时间/min | t1 | t2 | t3 | t4 | t5 |
CO2质量/g | 2.2 | 4.4 | 6.6 | 8.8 | 8.8 |
剩余固体质量/g | 22.8 | 20.6 | m | 16.2 | 16.2 |
则m=_____,t3时剩余固体中除杂质外含有的物质是_____(填化学式)
【题目】市场上的加碘食盐通常加入的是碘酸钾(KIO3),替代了原来的碘化(KI),因为碘化钾容易被氧气氧化。为探究不同条件下KI与O2的反应,进行如下系列实验。
(查阅资料)①碘单质(I2)遇淀粉液变蓝。②部分酸、碱、盐通常在水溶液中以离子形式存在,如:盐酸中存在H+和Cl-。
(进行实验)
实验1 将不同浓度的KI溶液置于纯氧中,放置相同时间后观察,现象如下表:
装置 | 烧杯中的液体 | 现象 |
| ①2 mL 0.15%KI溶液+5滴淀粉液 | 无明显变化 |
②2 mL 1.5%KI溶液+5滴淀粉液 | 溶液变蓝 | |
③2 mL 15%KI溶液+5滴淀粉液 | 溶液变蓝,颜色较②深 |
实验2 将相同浓度的KI溶液加入不同浓度的稀盐酸后置于纯氧中,5分钟后观察,现象如下表:
装置 | 烧杯中的液体 | 现象 |
| ④ 2 mL 15%KI溶液+5滴淀粉液+2mL蒸馏水 | 无明显变化 |
⑤ 2 mL 15%KI溶液+5滴淀粉液+2 mL1% 盐酸 | 溶液变蓝 | |
⑥ 2 mL 15%KI溶液+5滴淀粉液+2 mL 10% 盐酸 | 溶液变蓝,颜色较⑤深 |
(解释与结论)
(1)实验1的目的是___________________________。
(2)实验2中通过对比⑤和⑥,得出的结论是______________________。
(3)实验2中,KI在盐酸的作用下与O2反应的化学方程式如下,补全该反应的化学方程式:4KI+O2+4HCl=4KCl+2______+________。
(反思与评价)
(4)实验④中加2mL蒸馏水的作用是_____________________。
(5)某同学将实验⑥中2 mL10% 盐酸替换成2 mL10% NaCl溶液,5分钟后溶液颜色无明显变化,从离子角度分析,由此得出的结论是_________________________________。
【题目】在一支试管中放入一小段镁条(已擦去氧化膜),再向试管中加入一定量的盐酸,镁条表面有_____产生,反应的化学方程式是_____。
[发现问题]为了再次观察上述反应现象,小林同学用较长的镁条重做上述实验,但发现了异常现象,试管中出现了白色沉淀。
[实验验证1]小林同学针对两次实验的不同,设计对比实验方案,探究出现异常现象的原因。
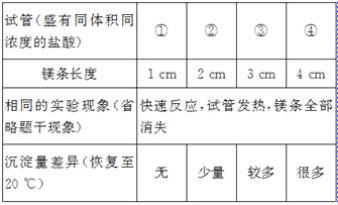
[得出结论]镁条与盐酸反应产生白色沉淀与_____有关。
[追问]白色沉淀是什么物质?
[查阅资料]①20 ℃时,100 g水中最多能溶解氯化镁54.8 g;
②镁能与热水反应产生一种碱和氢气;
③氯化银既不溶于水也不溶于稀硝酸。
[做出猜想]猜想一:镁;猜想二:氯化镁;猜想三:氢氧化镁,猜想的依据是_____(用化学方程式表示)。
[实验验证2]将白色沉淀洗涤干净,分别取少量沉淀于A、B、C试管中,进行如表实验:
试管 | 操作 | 现象 | 结论 |
A | 加入足量盐酸 | _____,白色沉淀_____ | 猜想一不正确,但这种白色沉淀能溶于盐酸 |
B | 加入足量水 | 白色沉淀_____ | 猜想二不正确 |
C | 加入适量稀硝酸 | 白色沉淀消失 | 原白色沉淀中含有的离子是:Mg2+、_____ |
继续滴加几滴硝酸银溶液 | 出现大量白色沉淀 |