题目内容
【题目】工业上以黄铜矿为原料,采用火法熔炼工艺生产铜,该工艺的中间过程会发生如下反应:
①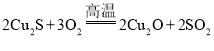 ;②
;②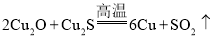
下列说法不正确的是
A.反应①中有三种元素的化合价发生了变化
B.生产原料除了黄铜矿,还会用到碱性物质
C.若得到的粗铜仅含少量铁杂质,可用硫酸铜溶液除去
D.在人类冶炼金属的历史上,炼铜早于炼铁
【答案】AB
【解析】
A、反应①中有两种元素的化合价发生了变化,硫元素的化合价从-2价变为+4价、氧元素的化合价由0价变为-2价,反应前后铜元素的化合价仍为+1价;故选项错误,但符合题意;
B、生产原料除了黄铜矿还会用到氧气,氧气不属于碱性物质;故选项错误,但符合题意;
C、杂质铁与硫酸铜溶液反应生成硫酸亚铁和铜,再经过过滤操作可以得到纯净的铜;故选项正确,但不符合题意;
D、人类冶炼和使用金属的历史与其活动性有关。越是活动性弱的金属,冶炼历史越早;故选项正确,但不符合题意。
故选:AB

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案【题目】兴趣小组的同学为探究碳酸钠的性质做了如下实验,请你一起完成。
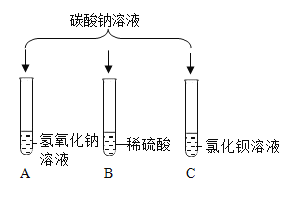
(1)试管A中没有发生反应,原因是__________________。
(2)试管B中的现象是_________________;试管C中发生反应的化学方程式为________________。
(3)上述实验结束后,该组同学将A、B、C三支试管中的废液倒入同--烧杯中,然后过滤得到滤液①,为确定滤液①的成分,同学们做了如下实验探究:
实验操作 | 实验现象 | 实验分析 | |
(4) | 取少量滤液①于试管中,向其中加入足量的氯化钡溶液,过滤,得到沉淀和滤液②, 向沉淀中加入足量稀硝酸 | 产生白 色沉淀; 加入稀硝酸后白色沉淀部分消失 | 根据实验现象可知,滤液②中一定含有_______________(填写溶质的化学式) |
(5) | 取少量滤液②于试管中,________________。 | ____________。 | 根据实验现象可知,滤液①中一定含有氢氧化钠 |
[实验结论](6)同学们通过分析推理,得出结论:滤液①中共含有_______________种溶质。
[实验反思](7)向滤液①中加入足量的氯化钡溶液的目的是________________。




