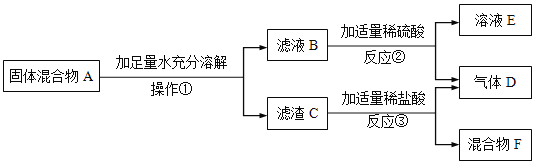
题目内容
【题目】甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是( )
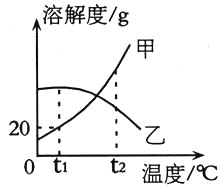
A.甲物质的溶解度为20g
B.t1℃时,30g甲加入到50g水中最多可得70g溶液
C.t2℃时,乙物质的饱和溶液升温变成不饱和溶液
D.t2℃,甲、乙两物质的饱和溶液分别降温到t1℃时,所得溶液中溶质质量分数的大小关系是:甲<乙
【答案】D
【解析】
A、甲物质的溶解度为20g是错误的,必须有温度的限制,故A错误;
B、t1℃时甲的溶解度为20g,说明该温度下,100g水中最多溶解20g,则50g水中最多溶解10g,所以t1℃时,30g甲加入到50g水中最多可得溶液质量为10g+50g=60g,故B错误;
C、t2℃时,乙物质的饱和溶液升温后溶解度变小,会析出晶体,所以仍然饱和,故C错误;
D、饱和溶液的质量分数:溶解度/(100g+溶解度)×100%,所以饱和溶液质量分数与溶解度有关,甲物质的饱和溶液降温到t1℃会析出晶体,变为饱和溶液,它的质量分数要按照t1℃甲物质的溶解度计算;乙降温后变为不饱和溶液,溶质质量分数不变,所以乙物质的质量分数按照t2℃时乙的溶解度计算就行,因为由溶解度曲线可知t1℃甲物质的溶解度小于t2℃时乙的溶解度,所以降温后所得溶液中溶质质量分数的大小关系是:甲<乙;故D正确。
故选D。

练习册系列答案
相关题目