题目内容
钠的化合物在日常生活中应用广泛。
(1)碳酸氢钠是发酵粉的成分之一,其俗称是 。
(2)次氯酸钠(NaClO)是84消毒液的有效成分,次氯酸钠中氯元素的化合价为 。
(3)氯化钠是重要的调味品,下面两幅示意图分别表示不同的化学反应,但生成物中都有氯化钠。


图1 图2
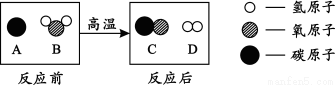
图1是钠与氯气反应生成氯化钠的示意图,氯化钠是由 (选填“原子”、“分子”或“离子”)构成的;由此看出,元素的化学性质与 密切相关。
图2描述了氢氧化钠溶液与盐酸反应的微观实质,该反应的基本反应类型为 。
(4)叠氮化钠(NaN3)被广泛应用于汽车安全气囊,汽车经撞击后,30毫秒内引发NaN3迅速分解生成两种单质,反应的化学方程式为 。
(1)小苏打 (2)+1
(3)离子 最外层电子数 复分解反应
(4) 2NaN3 撞击 2Na+3N2↑
【解析】
试题分析:(1)碳酸氢钠俗称小苏打,是发酵粉的主要成分;
(2)根据“在化合物中,正负化合价的代数和为零”的原则,已知Na的化合价为+1价,O的化合价为-2价,设次氯酸钠中氯元素的化合价为x,则(+1)+x+(-2)=0,解得x=+1;
(3)氯化钠是由钠离子和氯离子通过静电作用形成的离子化合物;元素的化学性质由最外层电子数决定;氢氧化钠溶液与盐酸反应生成的是氯化钠和水,反应物是两种化合物交换成分生成另两种化合物的反应属复分解反应;
(4)根据质量守恒定律化学反应前后元素的质量不变可知生成的是钠和氮气。
考点:钠及其化合物

(8分)牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答
问题。

【已知资料】
①SiO2不溶于水、且不与酸反应 ②K12、甘油、香精等均易溶于水
【实验探究】
Ⅰ:取一小段牙膏,加入蒸馏水,充分搅拌后静置,测得上层清液的pH为8.3,则此牙膏显 性。
Ⅱ:兴趣小组同学设计了如下实验方案,并进行3次实验。通过测量SiO2质量,从而确定此牙膏中SiO2的质量分数。实验过程如下:
①准确称取2.0g牙膏膏体,加足量水充分溶解并过滤。
②将滤渣转移至烧杯中,加入过量稀盐酸,至看到 为止。
③______、洗涤、干燥并称量得到剩余固体质量。(如表)
实验编号 | 1 | 2 | 3 |
实验前(g) | 2.00 | 2.00 | 2.00 |
实验后(g) | 0.43 | 0.44 | 0.45 |
④根据实验数据进行计算,此牙膏中SiO2
的质量分数为 %。
⑤反思实验过程。
A.步骤①中加足量水的目的是 。
B.步骤②中发生反应的化学方程式为 。
C.多次测量实验数据的目的是 。
D.若验证步骤②中盐酸过量,可以选择的试剂是 (至少写出类别不同的两种物质)。