��Ŀ����
����Ŀ��t1 ��ʱ����������������غ��Ȼ��طֱ���뵽ʢ��100 gˮ���ձ��У���ֽ����������ͼ1��ʾ������غ��Ȼ��ص��ܽ��������ͼ2��ʾ��������˵����ȷ����
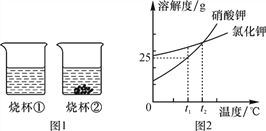
A. �ձ��ڵ���Һ������������Ϊ25%
B. �ձ��ٵ���Һ���������Һ
C. �ձ��ڵ���Һ���µ�t2 ��ʱ���ձ��ײ����в������ʲ��ܽ�
D. ���ձ��ٺ��ձ��ڵ���Һ�����µ�t2 ��ʱ�����ʵ������������
���𰸡�D
��������A���ձ��ڵĵײ��й���ʣ�࣬ʣ����Һ�DZ�����Һ����Һ������������=![]() 100%=20%����A����B��t1��ʱ����������������غ��Ȼ��طֱ���뵽��ʢ��100gˮ�������ձ��У���ֽ���ٵĵײ�û�й���ʣ�࣬�ڵĵײ��й���ʣ�࣬����t1��ʱ���ٵ��ܽ�ȴ��ڢڵ��ܽ�ȣ������ձ��ٵ���Һ���Ȼ�����Һ����B����C��t2��ʱ���ձ������ʵ��ܽ�ȴ���t1��ʱ�ձ������ʵ��ܽ�ȣ��ձ����е�������t1��ʱ��ȫ�ܽ⣬�ձ����е����ʵ��ܽ�����¶ȵ����߶�����������Һ���µ�t2��ʱ���ձ����е�����ȫ���ܽ⣬��C����D��t2��ʱ���ձ������ʵ��ܽ�ȴ���t1��ʱ�ձ������ʵ��ܽ�ȣ��ձ����е�������t1��ʱ��ȫ�ܽ⣬������t2��ʱ�����ձ��е�����ȫ���ܽ⣬���ʵ�����������ȣ���D��ȷ����ѡD��
100%=20%����A����B��t1��ʱ����������������غ��Ȼ��طֱ���뵽��ʢ��100gˮ�������ձ��У���ֽ���ٵĵײ�û�й���ʣ�࣬�ڵĵײ��й���ʣ�࣬����t1��ʱ���ٵ��ܽ�ȴ��ڢڵ��ܽ�ȣ������ձ��ٵ���Һ���Ȼ�����Һ����B����C��t2��ʱ���ձ������ʵ��ܽ�ȴ���t1��ʱ�ձ������ʵ��ܽ�ȣ��ձ����е�������t1��ʱ��ȫ�ܽ⣬�ձ����е����ʵ��ܽ�����¶ȵ����߶�����������Һ���µ�t2��ʱ���ձ����е�����ȫ���ܽ⣬��C����D��t2��ʱ���ձ������ʵ��ܽ�ȴ���t1��ʱ�ձ������ʵ��ܽ�ȣ��ձ����е�������t1��ʱ��ȫ�ܽ⣬������t2��ʱ�����ձ��е�����ȫ���ܽ⣬���ʵ�����������ȣ���D��ȷ����ѡD��

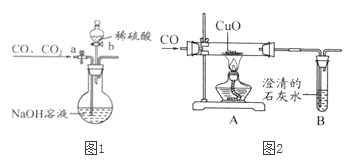
����Ŀ��С�������ͼ1��ʾ��ʵ��װ�ã���һ����̼��ԭ����ͭ�ķ�������CuO��Ʒ�Ĵ��ȣ�С��ȷ��ȡ��10g�������Ʒ����ʵ�顣�Իش�
��Ӧǰ | ��Ӧ�� | |
װ��A | 50g | 48.4g |
��1����װ�õIJ���֮����_______��
��2��ʵ�鿪ʼʱ����Ҫ���еIJ�����______������ţ���
��ͨһ����̼ �ڼ���
��3��ʵ������У�A���۲쵽��������______��B������ʯ��ˮ����ǵķ���ʽΪ______��
��4������ݱ��������CuO��Ʒ�Ĵ���Ϊ_______��
��5��Ϊ����Aװ���з�Ӧ�ų���һ����̼�Ͷ�����̼��С�����������ͼ2��ʾ��װ�ã�����̨�����еȹ̶�װ������ȥ��a��bΪ��������
�ٵ��رջ���b������aʱ���ɷ���õ�______��
��Ȼ��رջ���a���ٴ���b���ɷ���õ���һ�����塣