题目内容
现有一杯8%的氢氧化钠溶液50 g,丹丹同学向烧杯中倒入50 g稀硫酸后,用玻璃棒搅拌并测得完全反应后的溶液呈中性。2NaOH+H2SO4===Na2SO4+2H2O。
(1)反应后溶液的pH 7(选填“>”“=”“<”)。
(2)若将氢氧化钠溶液中溶质的质量分数变为原来的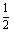 ,则应加入水为 g。
,则应加入水为 g。
(3)求上述反应后的溶液中溶质的质量分数。
(1)=
(2)50
(3)解:设反应后生成的Na2SO4质量为x
2NaOH+H2SO4====Na2SO4+2H2O
80 142
50g×8% x
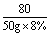 =
=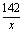 x=7.1g
x=7.1g
则反应后溶液中溶质的质量分数=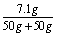 ×100%=7.1%
×100%=7.1%
(2)50
(3)解:设反应后生成的Na2SO4质量为x
2NaOH+H2SO4====Na2SO4+2H2O
80 142
50g×8% x
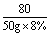 =
=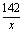 x=7.1g
x=7.1g则反应后溶液中溶质的质量分数=
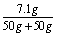 ×100%=7.1%
×100%=7.1%
练习册系列答案
相关题目
 ,则应加入水为 ______g.
,则应加入水为 ______g. ,则应加入水为 ______g.
,则应加入水为 ______g.