题目内容
【题目】空气中氧气含量测定的再认识。某化学兴趣小组的同学,在实验室用红磷、镁条、木炭等物质代替汞对空气中氧气的含量测定进行模拟探究。
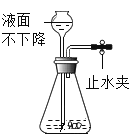
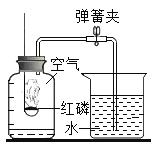
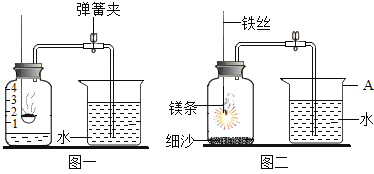
(实验一) A组同学通过燃烧红磷法测定空气中氧气的含量,装置如(图一)所示,写出红磷燃烧的符号表达式:____________________________________。
实验过程如下:
(1)用弹簧夹夹紧橡皮管;
(2)点燃燃烧匙内的红磷,观察到红磷燃烧,立即伸入瓶中并塞紧瓶塞;
(3)等装置冷却至室温后,打开弹簧夹;
(4)观察并记录水面的变化情况发现,集气瓶内上升的水面小于瓶内原有空气体积的五分之一,可能的一个原因是:____________________________________。
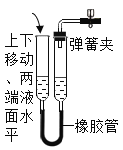
(实验二) B组同学利用镁条在空气中燃烧测定空气中氧气含量,如(图二)所示,实验结束后,待装置冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%。根据空气的组成推测可能的原因是____________________________________。
(实验三) C组”利用木炭燃烧测定空气中氧气的体积分数”,根据经验,利用上图装置测定空气中氧气含量时,能否用木炭替代?___________(填“能”或“不能”)原因是:______________________。
(提供资料)氢氧化钠能与二氧化碳反应生成碳酸钠和水
该小组同学选择用氢氧化钠溶液吸收生成的二氧化碳气体(如图三),但进入集气瓶中水的体积分数仍然小于1/5 。

(提出问题)是什么原因导致测量不准确呢?
(猜想与假设)他们分别作了如下猜想:
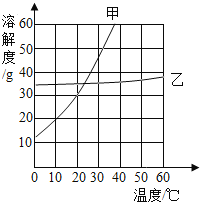
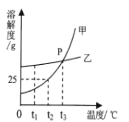
甲同学:可能是木炭取的量过少;
乙同学:可能是木炭燃烧没有消耗完集气瓶中的氧气;
丙同学:可能是木炭与空气反应生成了其他气体。
(查阅资料)
资料一:木炭、棉花和蜡烛在密闭容器内燃烧停止后,残留氧气的体积分数分别高达14.0%,8.0%和16.0%。
资料二:木炭在密闭容器中不充分燃烧会生成一氧化碳气体。
资料三:一氧化碳能与灼热的氧化铜粉末(黑色)反应生成铜(红色)和二氧化碳气体
(探究一)
小组同学发现实验结束后,燃烧匙中还有残留的黑色固体,可知__________同学的猜想不合理。
(探究二)乙同学又利用上述装置设计了如下实验,请你填写下表:
实验步骤 | 实验现象 | 实验结论 |
① 将足量木炭点燃,迅速插入装有氧气的 集气瓶中 | ______________ | 木炭燃烧没有 消耗完集气瓶 中的氧气 |
② 待装置冷却后,将燃着的___________ (填“棉花”或“蜡烛“)再伸入集气瓶中 | _______________ |
(探究三)
小明从木炭燃烧产物的角度猜想还可能是生成了_________________导致测量结果小于1/5;于是用注射器抽取集气瓶内的气体做了上图(图四)所示的实验,当观察到d中________________________(填实验现象),可证明小明的猜想成立。
(经典对比)通过与上述实验对比,拉瓦锡选择用汞的优点有_________________
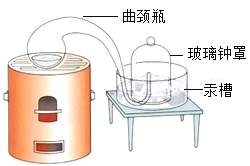
A 能将密闭装置内空气中的氧气几乎耗尽
B 在汞槽中起到液封作用
C 实验过程中没有污染
D 生成的化合物加热分解又能得到汞和氧气
【答案】P+O2![]() P2O5 红磷量不足或装置漏气或未等到装置冷却到室温就打开弹簧夹 空气中的氮气发生了反应 不能 木炭燃烧产生二氧化碳气体,没有产生压强差 甲 发出白光 棉花 棉花燃烧 一氧化碳 澄清石灰水变浑浊 ABD
P2O5 红磷量不足或装置漏气或未等到装置冷却到室温就打开弹簧夹 空气中的氮气发生了反应 不能 木炭燃烧产生二氧化碳气体,没有产生压强差 甲 发出白光 棉花 棉花燃烧 一氧化碳 澄清石灰水变浑浊 ABD
【解析】
根据测定空气中氧气含量实验的药品选择、装置、步骤、现象、结论、测定空气中氧气含量实验改进等多方面进行分析。
[实验一]红磷燃烧生成五氧化二磷,符号表达式: P+O2![]() P2O5;
P2O5;
集气瓶内上升的水面小于瓶内原有空气体积的五分之一,可能的一个原因是:红磷量不足(装置漏气或者未等到装置冷却到室温就打开弹簧夹)。
[实验二]氮气占空气体积的78%,推测可能的原因是空气中的氮气发生了反应。
[实验三]不能;原因是:木炭燃烧产生二氧化碳气体,没有产生压强差。
[探究一]
小组同学发现实验结束后,燃烧匙中还有残留的黑色固体,可知甲同学的猜想不合理。
[探究二]
将足量木炭点燃,迅速插入装有氧气的集气瓶中,现象:发出白光,放出热量;
待装置冷却后,将燃着的棉花;棉花燃烧。
[探究三]
小明从木炭燃烧产物的角度猜想还可能是生成了一氧化碳,导致测量结果小于1/5;于是用注射器抽取集气瓶内的气体做了上图(图四)所示的实验,当观察到d中澄清石灰水变浑浊,可证明小明的猜想成立。
[经典对比]通过与上述实验对比,拉瓦锡用汞的优点有:能将密闭装置内空气中的氧气几乎耗尽,在汞槽中起到液封作用,生成的化合物加热分解又能得到汞和氧气;汞有毒。故选ABD。

 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案