题目内容
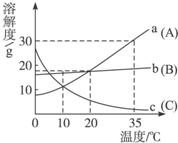 6、A、B、C三种固体物质的溶解度曲线如图所示.据图完成下列问题:
6、A、B、C三种固体物质的溶解度曲线如图所示.据图完成下列问题:(1)升高温度,接近饱和的
C
物质溶液会变得饱和.(2)10℃时,三种物质溶解度大小关系为:
B>A=C
.(3)35℃时,A物质的饱和溶液中:溶质、溶剂、溶液的质量比为
3:10:13
.(4)20℃时,25 g B物质放入到盛100 g水的烧杯中,充分溶解后溶液是
饱和
(填“饱和”或“不饱和”)溶液.(5)20℃时,取100 g A物质的饱和溶液,将温度升高到35℃,此时溶液中溶质的质量分数是
不变
(填“变大”“变小”或“不变”).(6)要将A从它的饱和溶液中结晶出来,最好采取
降温结晶
的方法,而要将B从它的饱和溶液中大量析出,最好采取蒸发溶剂结晶
的方法.分析:由溶解度曲线图可知,不同物质的溶解度在同一温度时的大小情况,也能知道同一物质的溶解度受温度的影响情况.
解答:解:(1)由溶解度曲线图可知A、B、C三种固体物质的溶解度只有C的溶解度随温度的升高而降低,所以当升温时,C的不饱和溶液能变为饱和溶液.
(2)由溶解度曲线图可知,10℃时三种物质溶解度大小关系:B>A=C.
(3)35℃时,A物质的溶解度为30g,由此可知30gA在100g水中恰好达饱和形成130g溶液,故A物质的饱和溶液中:溶质、溶剂、溶液的质量比为3:10:13.
(4)20℃时,B物质的溶解度为18g,故25 g B物质放入到盛100 g水的烧杯中,只能溶解18g,所以所得溶液为饱和溶液.
(5)20℃时,取100 g A物质的饱和溶液,将温度升高到35℃时,因A的溶解度随温度的升高而升高,所以溶液会由饱和溶液变为不饱和溶液,但溶液中溶质的质量分数保持不变.
(6)因A的溶解度受温度影响较大,所以要将A从它的饱和溶液中结晶出来,最好采取降温结晶的方法.而B的溶解度受温度影响较小的,所以要将B从它的饱和溶液中大量析出,最好采取蒸发溶剂法.
故答案为:(1)C.
(2)B>A=C.
(3)3:10:13.
(4)饱和.
(5)不变.
(6)降温结晶;蒸发溶剂结晶.
(2)由溶解度曲线图可知,10℃时三种物质溶解度大小关系:B>A=C.
(3)35℃时,A物质的溶解度为30g,由此可知30gA在100g水中恰好达饱和形成130g溶液,故A物质的饱和溶液中:溶质、溶剂、溶液的质量比为3:10:13.
(4)20℃时,B物质的溶解度为18g,故25 g B物质放入到盛100 g水的烧杯中,只能溶解18g,所以所得溶液为饱和溶液.
(5)20℃时,取100 g A物质的饱和溶液,将温度升高到35℃时,因A的溶解度随温度的升高而升高,所以溶液会由饱和溶液变为不饱和溶液,但溶液中溶质的质量分数保持不变.
(6)因A的溶解度受温度影响较大,所以要将A从它的饱和溶液中结晶出来,最好采取降温结晶的方法.而B的溶解度受温度影响较小的,所以要将B从它的饱和溶液中大量析出,最好采取蒸发溶剂法.
故答案为:(1)C.
(2)B>A=C.
(3)3:10:13.
(4)饱和.
(5)不变.
(6)降温结晶;蒸发溶剂结晶.
点评:当把一定量的溶质放入一定量的溶剂中时,所得溶液的质量不一定等于所加溶质的质量加溶剂的质量.因为我们还要考虑溶解度情况.

练习册系列答案
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目

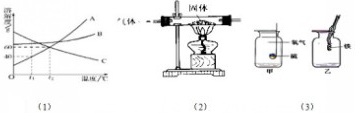
(I)图(1)是 A、B、C三种固体物质的溶解度曲线.
请回答:
(1)t1℃时,A、B、C三种物质的溶解度由大到小的顺序是______;
(2)当温度从t2℃降到t1℃时,三物质的饱和溶液中没有晶体析出的是______.
(II)用图(2)中的装置可进行气体和固体的反应.
(1)请在下表中写出两组不同的反应物(两组气体必须各不相同).
| 组别 | 固 体 | 气 体 |
| 1 | ______ | ______ |
| 2 | ______ | ______ |

(I)图(1)是 A、B、C三种固体物质的溶解度曲线.
请回答:
(1)t1℃时,A、B、C三种物质的溶解度由大到小的顺序是 ;
(2)当温度从t2℃降到t1℃时,三物质的饱和溶液中没有晶体析出的是 .
(II)用图(2)中的装置可进行气体和固体的反应.
(1)请在下表中写出两组不同的反应物(两组气体必须各不相同).
| 组别 | 固 体 | 气 体 |
| 1 | ||
| 2 |