题目内容
【题目】小明利用稀硫酸与某金属的反应来探究影响化学反应速率的因素,如表是五组5mL稀硫酸与0.lg某金属反应的实验数据(丝状金属的规格相同)分析上述数据,回答下列问题。
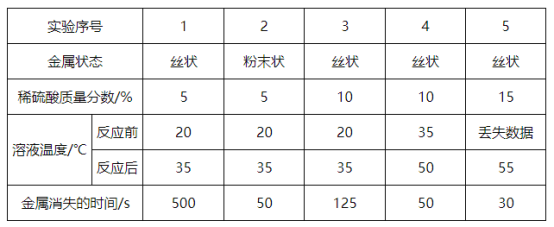
(1)小明是比较分析______来判断反应的速率。
(2)通过实验1和3,可得出的实验结论是______。
(3)依据实验规律,推测。丢失数据“的值约是______。
【答案】金属消失的时间 反应物浓度越大,化学反应越快 35℃
【解析】
(1)金属与稀硫酸反应,金属是反应物,随着反应的进行,反应物的质量逐渐减少,金属消失的时间越短,表示反应速率越快。由表中的数据可知,小明是比较分析金属消失的时间来判断反应的速率。故填:金属消失的时间;
(2)由实验1、3可知,金属的状态相同,反应物浓度越大,化学反应越快;故填:反应物浓度越大,化学反应越快;
(3)实验5是控制温度不变探究反应物的浓度对反应速率的影响,所以“丢失数据”的值约是35℃。故填:35℃。

练习册系列答案
相关题目