题目内容
【题目】在宏观、微观和符号之间建立联系是化学学科的特点。
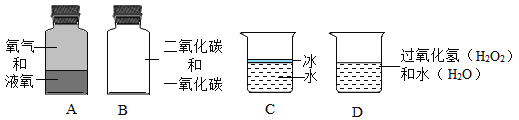
(1)在氧气、汞和氯化钠3种物质中,由离子构成的是_____。
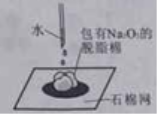
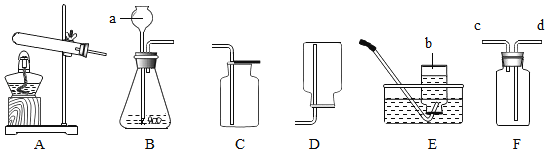
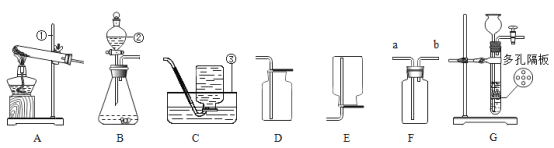
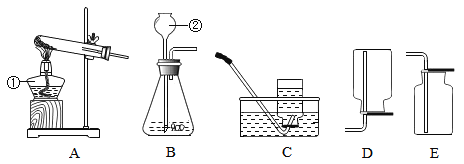
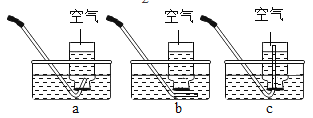
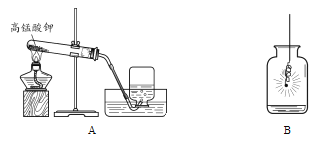
(2)下图所示的2个实验,从微观粒子的角度分析,两种变化的本质区别是_____,通过B实验证明水是由____组成的。
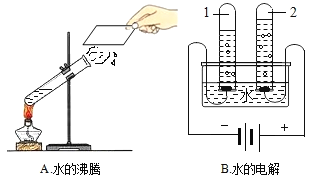
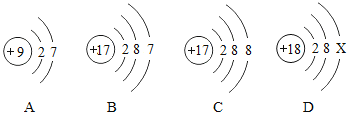
(3)A、B、C、D表示4种物质,其微观示意图见下表。A和B在催化剂作用下反应可生成C和D。下列说法正确的是____(填序号)。
反应前 | 反应后 |
| ||
A | B | C | D | |
|
|
|
| |
①4种物质均由分子构成 ②4种物质中D属于单质 ③该反应属于化合反应 ④反应前后各元素化合价均未改变 ⑤生成C、D两种物质的质量比为22:7,上述的化学方程式_____
【答案】氯化钠 A中分子没发生改变,B中分子本身发生改变 氢元素和氧元素 ①②⑤ 2CO+2NO 2CO2+N2
2CO2+N2
【解析】
(1)氧气是由氧气分子构成的;汞属于金属单质,是由汞原子直接构成的;氯化钠是由钠离子和氯离子构成的.
(2)水的沸腾水分子本身并没有发生变化,只是分子之间的间隔发生了变化,而电解水则是水分子分解生成了氢分子与氧分子,电解水的实验可证明水是由氢氧两种元素组成的;
(3)依据反应前后分子的结构可知该反应的方程式为:2CO+2NO 2CO2+N2,可知四种物质均由分子构成,只有D物质含有一种元素是单质,该反应的生成物有两种,不符合化合反应多变一的特征,所以不是化合反应,反应前后氮元素和碳元素的化合价均发生了改变,生成物CD的质量比是(2×44):28=22:7;
2CO2+N2,可知四种物质均由分子构成,只有D物质含有一种元素是单质,该反应的生成物有两种,不符合化合反应多变一的特征,所以不是化合反应,反应前后氮元素和碳元素的化合价均发生了改变,生成物CD的质量比是(2×44):28=22:7;
故答案为:
(1)氯化钠;
(2)A中分子没发生改变,B中分子本身发生了改变; 氢元素和氧元素;
(3)①②⑤;2CO+2NO 2CO2+N2.
2CO2+N2.

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案【题目】合成氨是人类科学技术上得一项重大突破,对社会发展与进步做出了巨大贡献。合成氨的工艺流程图如下:

(1)合成氨需要的氮气来自空气,空气中氮气的体积分数约为____。
(2)制取氢气的反应过程为:C+H2O![]() CO+H2。上述化学方程式中表现还原性的物质是___(填化学式)。
CO+H2。上述化学方程式中表现还原性的物质是___(填化学式)。
(3)写出N2、H2反应生成NH3的化学方程式_____,属于____反应。(填“化合反应”或“分解反应” )
(4)将沸点不同的气体分离开来,常采用液化分离法。如,控制温度在-183℃时,可将空气中N2与O2分离。根据下表中物质的沸点判断,要将产物NH3与N2、H2分离开来,最适宜的温度应该控制在_____℃。
物质 | H2 | N2 | O2 | NH3 |
沸点 | -252℃ | -195.8℃ | -183℃ | -33.35℃ |