题目内容
【题目】今有铜、锌混合物20g,该混合物恰好与200g稀盐酸中完全反应,生成0.4g氢气。试回答:
(1)铜、锌混合物中金属锌的质量为多少_______?
(2)该稀盐酸中溶质的质量分数为多少_______?(精确到0.1%)
(3)反应后溶液中溶质的质量分数为多少_______?(精确到0.1%)
【答案】13g 7.3% 12.8%
【解析】
根据生成的氢气的质量和对应的化学方程式求算锌的质量以及氯化锌的质量和该稀盐酸中溶质的质量分数,进而求算所得溶液中氯化锌的质量分数。
解:设锌的质量为x,生成的氯化锌的质量为y,该稀盐酸中溶质的质量分数为z,
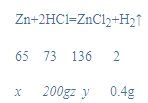
![]() x=13g,
x=13g,
![]() y=27.2g,
y=27.2g,
![]() z=7.3%,
z=7.3%,
反应后溶液中溶质的质量分数为![]() ×100%≈12.8%;
×100%≈12.8%;
答:(1)铜、锌混合物中金属锌的质量为13g;
(2)该稀盐酸中溶质的质量分数为7.3%;
(3)反应后溶液中溶质的质量分数为12.8%。

练习册系列答案
相关题目