题目内容
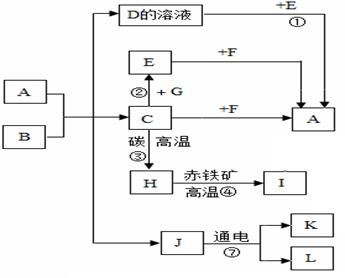
(2013四川成都)对比学习有利于发现事物的共性与个性。为探究酸的性质,同学们进行了如下实验。
清洗试管时,小乔同学将C、F两试管中的无色液体同时倒入一个洁净的废液缸,废液缸中立刻冒气泡并出现白色沉淀。请分析上述现象并回答:
Ⅰ.废液缸中产生气体的化学方程式为 (7) 。
Ⅱ. 废液缸里最终产生的白色沉淀中一定有硫酸钡,可能有 (8) (填化学式)。
| 实验内容 | 实验现象 | 分析与结论 |
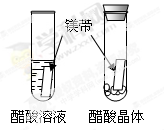 | 醋酸晶体试管内 (1),醋酸溶液试管中镁带表面冒气泡。 | 酸的很多反应通常在水溶液中才能完成。 |
用玻璃棒蘸硫酸在白纸上写字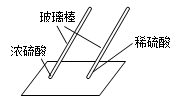 | (2)(填“浓”或“稀”)硫酸使白纸炭化。 | 即使是同种酸,由于(3) 不同,它们的性质不完全相同。 |
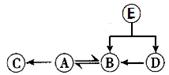
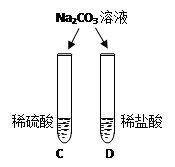 | 两试管中均产生(4) | 不同的酸具有相似的性质,这是因为酸的组成中都含有 (5)(填元素符号)。 |
 | E试管中产生 (6) , F试管中无明显现象。 | 不同的酸根会导致酸的“个性”差异。因此,可用氯化钡溶液鉴别盐酸和硫酸。 |
清洗试管时,小乔同学将C、F两试管中的无色液体同时倒入一个洁净的废液缸,废液缸中立刻冒气泡并出现白色沉淀。请分析上述现象并回答:
Ⅰ.废液缸中产生气体的化学方程式为 (7) 。
Ⅱ. 废液缸里最终产生的白色沉淀中一定有硫酸钡,可能有 (8) (填化学式)。
(1)无现象或无明显现象;(2)浓;(3)浓度或溶质质量分数等合理答案 (4)气泡; (5)H或H+;(6)白色沉淀 (7) Na2CO3 +2HCl ="2NaCl" +H2O +CO2↑ (8) BaCO3
试题分祈:(1)醋酸晶体不与镁反应,所以无明显现象.
(2)浓硫酸有脱水性,可使纸张炭化.
(3)浓硫酸浓度大,有脱水性;稀硫酸浓度小,无脱水性;可看出由于浓度不同二者的性质不完全相同
(4)碳酸钠可与稀硫酸、稀盐酸反应,均生成二氧化碳气体,因此都有气泡出现.
(5)酸具有相似的化学性质是因为在酸溶液中都含有大量的氢离子.
(6)硫酸可与氯化钡反应生成不溶于水的硫酸钡,所以E试管中会出现白色沉淀.
(7)根据上面的实验过程可知,废液中可能含有:Na2CO3 H2SO4 HCl BaCl2中未完全反应的物质.产生气泡说明废液中含有地Na2CO3 HCl. 二者反应:Na2CO3 +2HCl ="2NaCl" +H2O +CO2↑
(8)废液混合后出现白色沉淀说明废液中含有BaCl2 Na2CO3, 二者反应后会生成BaCO3;所 以还可能有BaCO3.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目