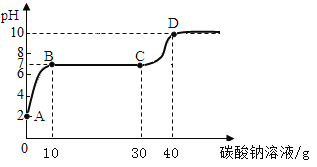
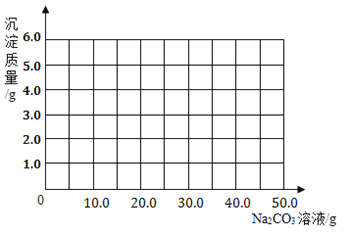
��Ŀ����
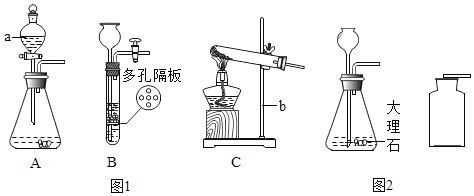
����Ŀ����ͼΪʵ���ҳ��õ�ʵ��װ�ã��ش����⣺
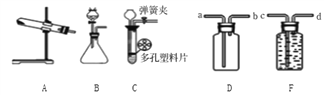
(1)д����KClO3��MnO2����ȡO2�Ļ�ѧ����ʽ��_________________________������Aװ����Ϊ����װ�ã���ȱ��______________(����������)����Ҫ�ռ��ϴ�������������Ӧ�������____(ѡ�a����b����c����d��)ͨ�롣
(2)ʵ������п����ϡ���ᷴӦ��ȡ����������װ����Cͼ��ʾ����ֹˮ�У�������ϡ����δ�����п����ϰ���п���Ӵ�������ʱ����ϡ����ɼӣ���������Һ�У������˴ӳ���©�������ӵ���_________(����ĸ)��
A������������Һ B��̼������Һ C����������Һ D������ʯ��ˮ
(3)С��ͬѧ���������ͼ��ʾ��ʵ��װ�ã��ȿ�������ȡCO2���ֿ�����̽��CO2�����ʡ�
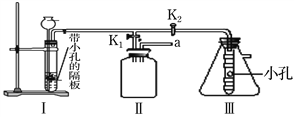
˵������װ������ʢ�ŵ�ҩƷ��ʯ��ʯ��ϡ���ᡣ��װ��������С�Թ��������4Ƭ��ֽ���������˵���Ƭ����ɫʯ����Һ��ʪ���м���Ƭ����ɫʯ����Һ������ɹ�ɡ�
a��ʵ��ʱ����K1�ر�K2��������ȡCO2��װ�â��з����Ļ�ѧ��Ӧ�Ļ�����Ӧ����Ϊ__��װ�â���ŵ���____________________________�������ſ������ռ�CO2���뽫ͼ�����������ڢ��з���___________���������ڼ���CO2��
b��ʵ��ʱ���ر�K1��K2������̽��CO2�����ʡ�ʵ��ʱ���г��ֵ�������________��
���𰸡� 2KClO3![]() 2KCl+3O2�� �ƾ��� �� d C ���ֽⷴӦ �� ���Ʒ�Ӧ�Ŀ�ʼ��ֹͣ �� ����ʯ��ˮ �� ������ֽ�ޱ仯��ʪ����ֽ�����������α��
2KCl+3O2�� �ƾ��� �� d C ���ֽⷴӦ �� ���Ʒ�Ӧ�Ŀ�ʼ��ֹͣ �� ����ʯ��ˮ �� ������ֽ�ޱ仯��ʪ����ֽ�����������α��
��������(1) KClO3��MnO2�����������ȷֽ������Ȼ��غ���������ѧ����ʽ��2KClO3 ![]() 2KCl+3O2��������Aװ����Ϊ����װ�ã���ȱ�پƾ��ƣ���Ҫ�ռ��ϴ�������������Ӧ������ˮ���ռ������������������ܶȱ�ˮ��С����Ӧ�������dͨ�룻(2)��п����ϡ���ᷴӦ��ȡ���������Լ�����Լ����������ᷴӦ��A������������Һ�����ᷴӦ�������������ƺ�ˮ������ B��̼������Һ�����ᷴӦ���������ƺ�ˮ��������̼������ C����������Һ�������Ӧ����ȷ�� D������ʯ��ˮ�����ᷴӦ��������ƺ�ˮ�����������˴ӳ���©�������ӵ��������ƣ�(3)ʯ��ʯ����Ҫ�ɷ�̼��ƺ�ϡ���ᣬ��Ӧ�����Ȼ��ơ�������̼��ˮ���Ǹ��ֽⷴӦ��װ�â���ŵ��ǿ��Ʒ�Ӧ�Ŀ�ʼ��ֹͣ���رյ��ɼУ���������ѹǿ�����Թ���Һ���½����½��������·������Һ����룬��Ӧֹͣ�����ɼУ�������٣�ѹǿ��С��©����Һ���½����Թ���Һ����������������Һ��Ӵ�ʱ����Ӧ��ʼ�������ſ������ռ�CO2�����ڶ�����̼���ܶȱȿ���������Ӧ�ӳ��ܽ��������ӳ��ܳ������ڢ��з������ʯ��ˮ���������ڼ���CO2��b��ʵ��ʱ���ر�K1��K2��ʵ��ʱ���г��ֵ������Ǹ�����ֽ�ޱ仯��ʪ����ֽ�����������α�죬֤��������̼���ܶȱȿ������ܺ�ˮ��Ӧ����̼�ᡣ
2KCl+3O2��������Aװ����Ϊ����װ�ã���ȱ�پƾ��ƣ���Ҫ�ռ��ϴ�������������Ӧ������ˮ���ռ������������������ܶȱ�ˮ��С����Ӧ�������dͨ�룻(2)��п����ϡ���ᷴӦ��ȡ���������Լ�����Լ����������ᷴӦ��A������������Һ�����ᷴӦ�������������ƺ�ˮ������ B��̼������Һ�����ᷴӦ���������ƺ�ˮ��������̼������ C����������Һ�������Ӧ����ȷ�� D������ʯ��ˮ�����ᷴӦ��������ƺ�ˮ�����������˴ӳ���©�������ӵ��������ƣ�(3)ʯ��ʯ����Ҫ�ɷ�̼��ƺ�ϡ���ᣬ��Ӧ�����Ȼ��ơ�������̼��ˮ���Ǹ��ֽⷴӦ��װ�â���ŵ��ǿ��Ʒ�Ӧ�Ŀ�ʼ��ֹͣ���رյ��ɼУ���������ѹǿ�����Թ���Һ���½����½��������·������Һ����룬��Ӧֹͣ�����ɼУ�������٣�ѹǿ��С��©����Һ���½����Թ���Һ����������������Һ��Ӵ�ʱ����Ӧ��ʼ�������ſ������ռ�CO2�����ڶ�����̼���ܶȱȿ���������Ӧ�ӳ��ܽ��������ӳ��ܳ������ڢ��з������ʯ��ˮ���������ڼ���CO2��b��ʵ��ʱ���ر�K1��K2��ʵ��ʱ���г��ֵ������Ǹ�����ֽ�ޱ仯��ʪ����ֽ�����������α�죬֤��������̼���ܶȱȿ������ܺ�ˮ��Ӧ����̼�ᡣ