题目内容
【题目】某化学兴趣小组同学欲除去固体氯化钠中混有的氯化钙,设计实验方案如下,请参与实验并回答问题。
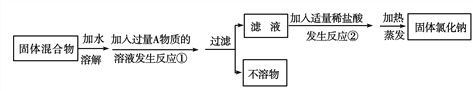
(1)写出A物质的化学式_____________,写出A物质的俗称_____________。
(2)写出反应②的化学方程式_________________________________________。
(3)反应①中加入过量A物质的目的是_________________________________。
反应②中如果加入盐酸也过量,则对所得到的氯化钠纯度________ (填“有”或“没有”)影响。
(4)分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果________ (填“增大”、“不变”或“减小”),其原因是_______________;你认为加入适量盐酸应依据的现象是_______________。
【答案】 Na2CO3 纯碱 Na2CO3+2HCl===2NaCl+H2O+CO2↑ 使氯化钙完全反应(合理即可) 没有 增大 加入过量的碳酸钠与盐酸反应也生成氯化钠 滤液中无气泡产生
【解析】本题考查了化学实验方案设计与评价,酸、盐的性质,化学方程式的书写。认真分析,根据条件综合把握化学反应。
(1)要除去氯化钠中的少量杂质氯化钙,只要除去钙离子就可以了,氯离子不是杂质。因此可以加入足量是碳酸钠溶液,生成白色沉淀碳酸钙,从而除去钙离子。碳酸钠的俗名是纯碱或苏打,化学式为:Na2CO3;
(2)②中的反应是碳酸钠与稀盐酸的反应,它们互相交换成分生成氯化钠和水和二氧化碳,化学方程式是Na2CO3+2HCl===2NaCl+H2O+CO2↑;
(3)反应①中加入过量A物质的目的是使氯化钙完全反应;反应②中如果加入盐酸也过量,盐酸具有挥发性并且是液体,通过加热蒸发即可除去,对所得的氯化钠的纯度无影响;
(4)分离后所得氯化钠的质量与原来氯化钠的质量相比较增多了,原因是每一步除杂质的过程中都生成了氯化钠;碳酸钠与盐酸结束后无气泡产生,加入适量盐酸应依据的现象是加HCl至刚好无气泡产生。

 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案