题目内容
【题目】根据下列实验装置图:“如图1”,回答有关问题.
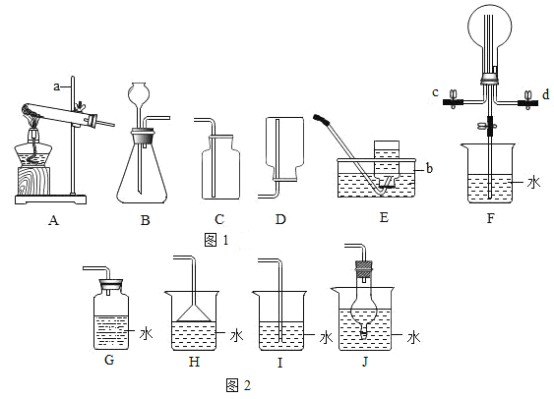
(1)写出图中标有仪器的名称:b_________;
(2)实验室用加热氯酸钾和二氧化锰的混合物制取氧气的化学方程式为____,选择的发生装置是____(填字母,下同),若得到较纯净的氧气,选择的收集装置是____;
(3)氨气是无色、有强烈刺激性气味的气体,密度比空气小,极易溶于水.实验室常用加热氯化铵和熟石灰混合物制取氨气,制取氨气的装置组合是____(填字母);
(4)某化学实验小组利用F装置收集氨气,并研究氨气的性质(部分仪器已略去)
①收集氨气时,氨气的进气口是____(填“c”或“d”) ;
②收集氨气后,进行探究氨气的性质实验,观察到烧瓶内产生了喷泉,说明氨气具有的性质是____;
③如图2为防止环境污染,G~J装置可用于吸收多余氨气的是____(填序号)。
【答案】水槽 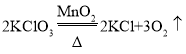 A E AD c 极易溶于水 HJ
A E AD c 极易溶于水 HJ
【解析】
(1)仪器b是水槽;
(2)氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气,该反应的化学方程式为: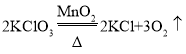 ;
;
该反应属于固体加热反应,发生装置应选A;
因为氧气的密度比空气大,氧气不易溶于水,可以用向上排空气法收集,即用C装置收集;也可以用排水法收集,即用E装置收集,用排水法收集的氧气比用排空气法收集的氧气纯净,故收集装置应选E;
(3)实验室常用氯化铵固体与碱石灰固体共热来制取氨气,该反应属于固体加热反应,发生装置应选A;
由于氨气密度比空气小,氨气极易溶于水,只能用向下排空气法收集,收集装置可选用D,故填:AD;
(4)①因为氨气的密度比空气小,收集氨气时,氨气的进气口是c;
②收集氨气一段时间后,打开F装置中的止水夹,观察到烧瓶内产生了喷泉,说明氨气具有的性质是氨气极易溶于水,使装置内压强减小,在外界大气压的作用下,形成喷泉,故填:极易溶于水;
③为防止环境污染,要吸收掉多余的氨气,吸收氨气后,会使装置内压强减小,容易产生倒吸,故选择的装置必须能够防止倒吸,H、J装置中的倒置的漏斗和球形干燥管的体积较大,能防止液体倒吸进入反应装置,可用于吸收多余氨气,故填:HJ。

 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案【题目】回收废旧干电池、保护环境是我们每个公民的义务,下面是某校兴趣小组探究旧电池组成的过程(片段),请帮助他们完成相应的实验报告.
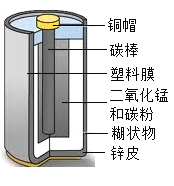
(提出问题)组成废旧干电池的物质是什么?
(查阅资料)淀粉遇碘变蓝
(活动探究1)电池主要由什么材料组成?金属材料:________________(请举一例)
(活动探究2)电池的糊状物中有没有我们熟悉的离子?
(猜想1)小组中的同学在剥开电池锌壳时,闻到一股淡淡的刺激性气味,因此他们猜想:电池的糊状物可能含有NH4+.
(设计方案1)取少量白色糊状物与____________混合、研磨,闻到氨味,证明上述猜想正确.
(猜想2)可能含有OH-、CO32-、Cl-中的一种或几种.
(设计方案2)为了验证猜想2,他们设计如下实验,请完成表格中相应内容.
实验操作 | 实验现象 | 实验结论 |
1、 取样,溶于适量的水中,静置,过滤, 取少量滤液于试管中,滴加紫色石蕊试液 | 石蕊试液不变蓝 | 没有____________ |
2、另取少量滤液于另一个试管中,滴加稍过量的稀硝酸 | ______________ | 没有CO32-存在 |
3、向第二步所得溶液中滴加__________ | 有白色沉淀产生 | 存在的离子是Cl- |
4、取白色糊状物,滴加少量碘液 | 溶液________ | 有淀粉存在 |
(结论)上述实验证明,电池内白色糊状物主要是 ___________和__________.
根据结论,写出方案1闻到氨味的反应方程式:_________________________________
(交流与讨论)若将上述步骤2中滴加稀硝酸改为滴加稀盐酸,你认为对本实验有无影响?说明你的理由______________________________________________.