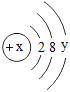题目内容
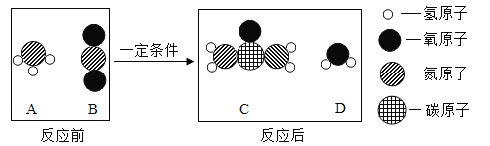
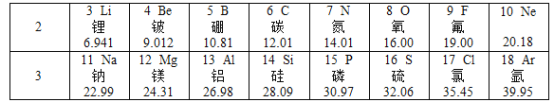
【题目】下表为元素周期表中部分元素的相关信息,利用下表回答相关问题。
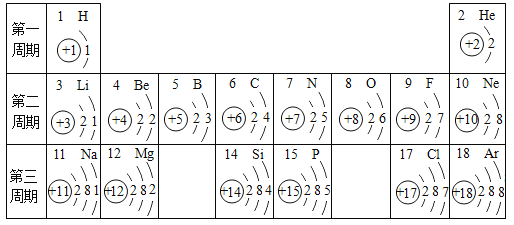
(1)请画出16号元素原子结构示意图__________________,化学反应中该原子比较容易________(选填“得到”或“失去”)电子变成离子。
(2)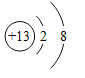 表示的是________(填化学符号)。
表示的是________(填化学符号)。
(3)仔细观察上表,我们能发现很多规律:
①同周期(同一横行)元素的原子核外____________数相同,____________________数从左到右依次递增;
②同族(同一纵行)元素的原子核外____________________数相同,____________数从上到下依次递增。
(4)相对原子质量与原子真实质量之间存在紧密的关系(见下表),根据下表判断6.02×1023个钠原子的质量y为______________。请归纳下表中的规律:6.02×1023个某原子的质量在数值上等于该原子的__________。
碳 | 氧 | 钠 | |
相对原子质量 | 12 | 16 | 23 |
6.02×1023个原子的质量 | 12g | 16g | y |
【答案】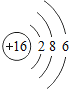 得到 Al3+ 电子层 最外层电子 最外层电子 电子层 23g 相对原子质量
得到 Al3+ 电子层 最外层电子 最外层电子 电子层 23g 相对原子质量
【解析】
(1)16号元素原子中,质子数为16,核外电子数为16,根据核外电子排布规律可知,第1层排2个电子,第2层排8个电子,第3层排6个电子,16号元素原子结构示意图: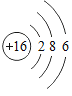 ,硫原子最外层有6个电子,化学反应中该原子比较容易得到电子变成离子;
,硫原子最外层有6个电子,化学反应中该原子比较容易得到电子变成离子;
(2)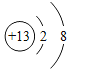 表示的是铝原子失去3个电子变为铝离子:Al3+;
表示的是铝原子失去3个电子变为铝离子:Al3+;
(3)①同周期(同一横行)元素的原子核外电子层数相同,最外层电子数从左到右依次递增;
②同族(同一纵行)元素的原子核外最外层电子数相同,电子层数从上到下依次递增。
(4)相对原子质量与原子真实质量之间存在紧密的关系,6.02×1023个碳原子的质量为12g,数值上与碳的相对原子质量相等;6.02×1023个氧原子的质量为16g,数值上与氧的相对原子质量相等;根据下表判断6.02×1023个钠原子的质量y为23g。表中的规律:6.02×1023个某原子的质量在数值上等于该原子的相对原子质量。

【题目】有一黑紫色的固体为KnMO4和MnO2的混合物,为测定混合物中KMnO4的质量,某同学取样35.0g,对固体充分加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):
反应时间/min | 1.0 | 2.0 | 3.0 | 4.0 | 5.0 |
剩余固体质量/g | 34.2 | 33.4 | 32.6 | 31.8 | 31.8 |
分析表中数据,完成下列问题:
(1)反应到___________min时反应完毕;
(2)该样品中KMnO4的质量_______。
【题目】下列化学方程式及其反应类型都正确的是
选项 | 化学方程式 | 反应类型 |
A | Mg+O2 | 化合反应 |
B | H2O2 | 分解反应 |
C | Fe+H2SO4=FeSO4+H2↑ | 置换反应 |
D | 2KNO3+Ba(OH)2=Ba(NO3)2+2KOH | 复分解反应 |
A.AB.BC.CD.D