题目内容
【题目】金属和我们的关系很密切,它广泛地存在和应用于生产、生活等各个领域。
(1)下图为我们提供了金属铝、金属铁两种元素在元素周期表中的一些相关信息。
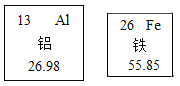
①铁原子核内的质子数为________________;
②铁元素相对原子质量为___________;
③铝的原子结构示意图为____________。
(2)乐乐兴趣小组在实验室进行实验探究:他们将两根完全相同的铝丝分别伸入到稀盐酸和稀硫酸中,观察发现铝丝产生气泡的快慢很是不同。
(提出问题)影响铝和酸反应速率的因素有哪些?
(大胆猜想)I.温度:
Ⅱ._______________:
Ⅲ.酸的种类。
(实验设计)为了验证猜想Ⅱ是否正确,乐乐兴趣小组的同学们进行了如下的实验探究。
实验步骤 | 实验观象 | 实验结论 |
打磨两根型号完全相同的铝丝,分别放入两支相同的试管中,再分别向其中倒入同体积、但不同浓度的稀盐酸 | ________________ | 酸的浓度越大,反应速率越快。 |
①上述反应的化学方程式为____________:
②使用铝丝前打磨的原因是___________。
③对铁质零件进行“发蓝”处理也是一种常用的防锈措施,因能在其表面形成致密氧化膜。若将该零件浸泡于硫酸铜溶液中,发现零件表面出现红色物质,便可以断定该铁质零件的“发蓝”处理效果不佳,原因是__________________。
(3)高铁的迅速发展对钢轨的需求量越来越大,质量要求越来越高。在工业上,经常用“铝热反应”原理来焊接钢轨,原理就是利用铝和氧化铁在高温条件下发生剧烈反应得到熔融的金属,其反应化学方程式为_____________。
【答案】26 55.85 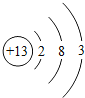 酸的浓度 金属铝与浓度较大酸反应产生气泡更多更快
酸的浓度 金属铝与浓度较大酸反应产生气泡更多更快 ![]()
![]()
![]()
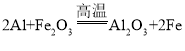
【解析】
(1)①在元素周期表中,元素名称左上角的数字表示原子序数,原子序数=质子数=26;
②在元素周期表中,元素名称下方的数字表示相对原子质量,故铁元素的相对原子质量为55.85;
③在元素周期表中,元素名称左上角的数字表示原子序数,原子序数=质子数=原子的核外电子数=13,故铝原子核外有13个电子、第一层为2个,第二层为8个,第三层为3个,故铝的原子结构示意图为: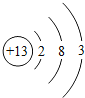 ;
;
(2)大胆猜想:由实验设计可知,该实验探究了不同浓度的酸对反应速率的影响,故猜想Ⅱ为:酸的浓度;
实验设计:实验结论为:酸的浓度越大,反应速率越快,故打磨两根型号完全相同的铝丝,分别放入两支相同的试管中,再分别向其中倒入同体积、但不同浓度的稀盐酸,酸的浓度越大,反应速率越快看,故实验现象为:金属铝与浓度较大的酸反应产生的气泡更多更快;
①铝与稀盐酸反应生成氯化铝和氢气,该反应的化学方程式为:![]() ;
;
②铝的化学性质比较活泼,在常温下,铝能与空气中的氧气反应,在其表面生成一层致密的氧化铝薄膜,故使用前,应打磨铝丝,防止影响实验进行,该反应的化学方程式为:![]() ;
;
③将该零件浸泡于硫酸铜溶液中,发现零件表面出现红色物质,说明铁与硫酸铜反应生成了硫酸亚铁和铜,该反应的化学方程式为:![]() ,由此说明铁的“发蓝”处理效果不佳;
,由此说明铁的“发蓝”处理效果不佳;
(3)铝和氧化铁在高温条件下发生剧烈反应得到熔融的金属,该金属为铁,根据质量守恒定律,化学反应前后,元素的种类不变,反应物中含铁、氧、铝元素,故另一生成物应为三氧化二铝,故该反应的化学方程式为: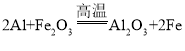 。
。

【题目】化学小组同学在课外读物中看到:“加热时,过氧化钠(Na2O2)能与木炭发生化学反应”。他们决定探究Na2O2与木炭反应的产物。
(猜想与假设)木炭与Na2O2反应可能生成4种物质:CO、CO2、Na2O和Na2CO3。
(查阅资料)
① 碱性的碳酸钠溶液与中性的CaCl2溶液能发生复分解反应。
② 氧化钠(Na2O)是白色固体,与H2O反应生成NaOH。
③ 氯化钯(PdCl2)溶液能检验CO的存在,向溶液中通入CO,产生黑色沉淀。
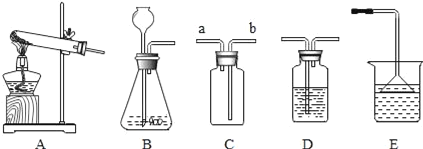
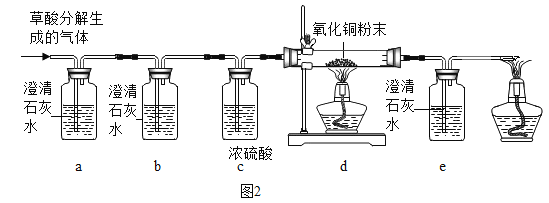
(进行实验)同学们在老师的指导下设计了如下图所示装置(部分夹持仪器已略去)。
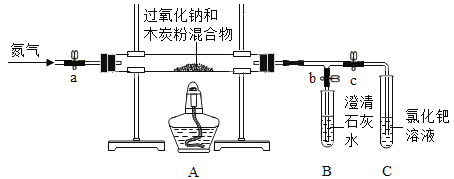
序号 | 实验操作 | 主要实验现象 | 实验结论 |
① | 检查装置气密性。向玻璃管中加入过氧化钠和过量木炭粉的混合物。打开弹簧夹a、b,关闭c,从装置左端通一段时间N2。 | A中无明显变化,B中有大量气泡冒出。 | 气密性良好。 |
② | 关闭a,点燃酒精灯。 | 试管中发生剧烈反应,产生火花,________________。 | 产物中没有CO2。 |
③ | 打开c,关闭b。 | C中PdCl2溶液没有明显变化。 | ___________________。 |
④ | 打开a,继续通N2,停止加热,待冷却后停止通N2。取出少量反应后固体于试管中,加入足量稀盐酸,迅速用带导管的橡胶塞塞紧试管口,导管另一端通入石灰水中。 | _____________________。 | 产物中有Na2CO3。 |
(解释与结论)
(1)检验第4种物质存在的实验方案:取出少量反应后固体于试管中,_______________,则第4种物质存在。
(2)Na2O2与木炭反应的化学方程式为_________________________________。
(反思与评价)实验操作④中若不通入N2,可能造成的结果是________________________。